Archiv für die Kategorie „Kongressberichte“
Innovationen in der Krebsdiagnostik
Fortschritte in der Krebsdiagnostik wurden auch beim Deutschen Krebskongress 2018 in Berlin vorgestellt.
Moderne Bildgebungsverfahren, die nicht nur die anatomische Lage eines Tumors abbilden, sondern auch funktionelle Informationen über den Tumor liefern, bringen deutliche Fortschritte in der Krebsversorgung. Das gilt zum Beispiel für die multiparametrische MRT bei der Diagnose des Prostatakarzinoms. Knapp 70.000 Männer erkranken jährlich daran neu. Die entscheidende Frage in der Primärdiagnostik lautet: Welcher Patient trägt einen rasch wachsenden aggressiven Tumor in sich, der unbedingt behandelt werden muss, und wo kann aufgrund eines niedrigen Risikoprofils zunächst mit der Behandlung abgewartet werden? Die multiparametrische Magnetresonanztomographie (mpMRT) ist das derzeit empfindlichste bildgebende Verfahren, um ein Prostatakarzinom abzubilden. Sie liefert zudem wichtige funktionelle Informationen, etwa über die Durchblutung des Tumors und seine Zelldichte, was wiederum Hinweise auf die individuelle Aggressivität gibt. Eine mpMRT kann damit sowohl anatomische als auch biologische Daten erfassen − die Ergebnisse tragen zu einer besseren Risikoabschätzung bei und ermöglichen eine gezielte Stanzbiopsie. Die mpMRT hat mittlerweile sogar Eingang die aktuelle Leitlinie des Leitlinienprogramms Onkologie gefunden, zum Beispiel, wenn nach einer negativen systematischen Biopsie der Verdacht auf ein Prostatakarzinom weiterbesteht oder wenn ein Patient die aktive Überwachung in Erwägung zieht.
Prof. Dr. Dipl.-Phys. Heinz-Peter Schlemmer, Deutsches Krebsforschungszentrum Heidelberg
Die Grenzen dieser Methode liegen dort, wo die Diagnose mit der MRT nicht hinreichend eindeutig ist: etwa beim Staging, wenn Lymphknotenmetastasen identifiziert werden sollen. Hier ist dieHybridbildgebung gefragt. In der Computertomographie (CT) oder der MRT können befallene Lymphknoten nur dann identifiziert werden, wenn sie eine bestimmte Größe erreicht haben. Bessere Resultate lassen sich in Kombination mit der Positronenemissionstomographie, kurz PET, erzielen. Die PET-MRT-Hybridbildgebung ist ein sehr aussichtsreiches Zukunftsfeld. Die strahlungsfreie MRT zeichnet sich durch einen hohen Weichteilkontrast aus, die Positronenemissionstomographie mit einem geeigneten Radiotracer ist hochempfindlich und kann deshalb selbst kleinste Tumorherde sichtbar machen.
Quelle: Pressemitteilung Deutscher Krebskongress 2018
Bewegungstherapie hocheffektiv
Neue Erkenntnisse zu Fatigue und Polyneuropathie beim 33. Deutschen Krebskongress 2018 in Berlin vorgestellt.
Viele Krebspatienten leiden unter den Nebenwirkungen ihrer Therapie. Dazu gehören etwa Erschöpfung, auch Fatigue-Syndrom genannt, oder Polyneuropathie, eine Schädigung der Nerven. Gezieltes bewegungstherapeutisches Training hilft, die zum Teil starken Einschränkungen zu reduzieren und die Lebensqualität der Betroffenen zu steigern. Aktuelle Studienergebnisse – unter anderem eine Meta -Analyse aus den USA – konnten nun belegen: Körperliche Aktivität vermindert die Beschwerden erfolgreicher als eine medizinische oder eine psychologische Therapie.
„Bewegung ist das geeignetste ‚Medikament‘ zur Reduzierung des Fatigue-Syndroms“, berichtete PD Dr. Freerk Baumann, Leiter der Arbeitsgruppe Onkologische Bewegungsmedizin am CIO Köln/Bonn. Doch nicht nur bei der Behandlung des Fatigue-Syndroms gibt es neue Erkenntnisse. „Auch bei der Chemotherapie-induzierten Polyneuropathie (CIPN) zeigen Studien, dass Bewegungstherapie hilft. Für die Polyneuropathie gibt es keine andere Behandlungsmethode, deren nachhaltige Wirkung bewiesen werden konnte“, so Baumann weiter. „Sensomotorisches Training und womöglich auch Vibrationstraining erzielen die besten Effekte bei der Therapie von Nervenschäden, wie eingeschränktes Tastgefühl an den Händen sowie Kribbeln und Schmerzen an Händen und Füßen.“ Dieser Ansatz wird derzeit in einer gemeinsamen Studie der Deutschen Sporthochschule Köln und der Uniklinik Köln weiter verfolgt. Erste Forschungsergebnisse unterstützen die Annahme, dass spezielles Bewegungstraining eine hemmende Wirkung auf die CIPN haben könnte.
Trotz der Erfolge, die mit einer gezielten Bewegungstherapie erreicht werden können, ist es jedoch schwierig, entsprechende Versorgungsstrukturen für alle Patienten zu schaffen. „Ein therapeutisches Training während der medizinischen Krebstherapie muss individuell auf die Patienten angepasst werden. Hierzu bedarf es speziell ausgebildeter Sport- und Physiotherapeuten, von denen es zurzeit noch nicht genügend gibt“, erklärte der Direktor des Centrums für integrierte Onkologie (CIO) Köln/Bonn, Professor Dr. Michael Hallek. „Darüber hinaus bestehen in den Onkologischen Zentren auch räumliche und finanzielle Engpässe, um hochwertige Trainingsgeräte anzuschaffen.“ Erschwerend käme hinzu, dass die Sporttherapie im Gegensatz zur Physiotherapie nicht im Heilmittelkatalog aufgeführt ist , obwohl die positiven Effekte durch Sporttherapie bereits sehr gut wissenschaftlich belegt seien.
„Hier ist die Gesundheitspolitik gefordert, dies schnellstens zu ändern“, unterstrich PD Dr. Baumann. „Denn, würde die Sporttherapie in den Heilmittelkatalog aufgenommen, so wäre es für die Krebszentren deutlich einfacher, entsprechende bewegungstherapeutische Strukturen aufzubauen.“ Um umfassende Informationen über die Versorgungsstrukturen zur Bewegungstherapie in Deutschland zu erhalten und Erkenntnisse darüber zu gewinnen, inwieweit Krebspatienten die Möglichkeiten der Sporttherapie überhaupt vermittelt werden, hat die Deutsche Krebshilfe eine bundesweite Umfrage bei über 700 Krebszentren durchgeführt. „Die Ergebnisse dieser Befragung werden in Kürze vorliegen, doch schon jetzt zeichnet sich dringender Handlungsbedarf ab“, erklärte Gerd Nettekoven, Vorstandsvorsitzender der Deutschen Krebshilfe.
„Das Thema körperliche Aktivität in der Krebstherapie hat für die Deutsche Krebshilfe einen hohen Stellenwert. Wir halten es für wichtig, die Forschung auf diesem Gebiet voranzutreiben, um weitere wissenschaftliche Erkenntnisse zu erhalten. Wir wollen aber auch Krebspatienten und Ärzte umfassend über die positiven Effekte der Bewegungstherapie informieren.
“ Dies gelte zudem nicht nur für die Zeit während der Therapie, sondern auch für die Zeit danach, denn auch in der Krebsnachsorge seien Sport und Bewegung wichtig für das Wohlbefinden der Betroffenen. Um das Thema Bewegung stärker und mit Nachhaltigkeit sowohl in der Therapie als auch in der Krebsnachsorge zu verankern, haben die Deutsche Krebshilfe, der Deutsche Olympische Sportbund und die Deutsche Sporthochschule Köln im Jahr 2014 die Initiative „Bewegung gegen Krebs“ gestartet.
Unterstützt werden sie dabei von Heiko Herrlich, ehemaliger Fußballprofi und heute Bundesligatrainer sowie Antje Möldner-Schmidt, Europameisterin im 3.000-Meter-Hindernislauf. Herrlich und Möldner-Schmidt wissen als ehemalige Patienten um die zentrale Bedeutung von Sport und Bewegung während und nach der Krebstherapie. „Für mich brach eine Welt zusammen, als ich mit der Diagnose Krebs konfrontiert wurde“, berichtete Möldner-Schmidt in Berlin. „Doch Sport und Bewegung haben mir sehr geholfen, die schwere Zeit durchzustehen und viele Hürden zu überwinden.“ Die Leichtathletin erkrankte im Januar 2010 an Morbus Hodgkin. Bereits zehn Monate nach der Diagnose nahm sie das Training wieder auf und wurde im Jahr 2014 Europameisterin.
Quelle: Presseinformation 33. Deutscher Krebskongress 2018, Pressestelle Deutsche Krebsgesellschaft und Pressestelle Stiftung Deutsche Krebshilfe e.V.
Aktuelle Entwicklungen in der Krebstherapie wurden von Onkologen im Rahmen ihrer Jahrestagung diskutiert
Die diesjährige Jahrestagung der Deutschen, Österreichischen und Schweizerischen Fachgesellschaften für Hämatologie und Medizinische Onkologie stand auch in diesem Jahr unter dem Eindruck der innovativen Diagnosemöglichkeiten und der vielen neuen Arzneimittel, vor allem bei Krebs, aber auch bei nicht bösartigen Blutkrankheiten. Gleichzeitig wird offen über Hemmnisse wie regulatorische Hürden, unzureichende Studien und fehlende Register diskutiert. Der von rund 5.700 teilnehmenden Expertinnen und Experten für medikamentöse Tumortherapie besuchte Kongress bietet eine wichtige Plattform zum Austausch über das neue Wissen und der zeitnahen Umsetzung im Behandlungsalltag.
Paradigmenwechsel: Vom Organ zum System
Mit den modernen Verfahren zur Tumordiagnostik wie dem Next Generation Sequencing oder der „liquid biopsy“, habe man die Wahl und die Steuerung der Behandlung bösartiger Erkrankungen deutlich verbessern können, so Prof. Andreas Hochhaus, diesjähriger Kongresspräsident und Direktor der Abteilung Hämatologie/Internistische Onkologie am Universitätsklinikum Jena. „Die neuen Diagnoseverfahren geben uns die Möglichkeit, die zur Verfügung stehenden innovativen Arzneimittel sehr gezielt einzusetzen.“ Derzeit erlebe die Häma-tologie und Onkologie einen Paradigmenwechsel von der organzentrierten Betrachtungsweise des Krebs hin zu einer organübergreifenden systemischen Perspektive beispielsweise basierend auf bestimmten genetischen Mutationen, die sich in Form verschiedener Tumorentitäten manifestierten. Diese systemische Betrachtungsweise führe auch dazu, dass bei modernen Therapien wie der Immuntherapie, dem organunabhängigen Nebenwirkungsmanagement eine wichtigere Bedeutung zukomme, so Hochhaus weiter.
Zentrale Aspekte der Hämatologie
Der Kongresspräsident warb für eine Besinnung auf die zentralen Aspekte der Hämatologie wie z. B. die Morphologie und die Blutgerinnung, betonte aber gleichsam, dass dies nicht rückwärtsgewandt zu verstehen sei. „Bei aller Wissenszunahme und bei aller Innovationskraft dürfen wir die zentralen Aspekte unseres Faches nicht aus dem ärztlichen Blick verlieren“, so Hochhaus weiter. Hierfür stehe auch das Motto der Jahrestagung ‚Blut ist ein ganz besonderer Saft‘. Der Kongresspräsident betonte, dass diese Entwicklung Hand in Hand mit der Nachwuchsförderung in der Hämatologie und Onkologie gehen müsse. „Die Zukunft unseres Fachgebietes können wir nur mit hochqualifiziertem ärztlichen und wissenschaftlichen Nachwuchs sichern, der den aktuellen Stand des Wissens kennt und die Umsetzung in Diagnose und Therapie im Behandlungsalltag beherrscht. Dabei ist es kein Widerspruch, wenn unsere jungen Kolleginnen und Kollegen auch nach wie vor die Morphologie von Zellen mit Hilfe des klassischen Lichtmikroskops beurteilen können“, so Hochhaus.
Interkulturelle Aspekte der Hämatologie
Im Rahmen der Pressekonferenz verwies Hochhaus auch auf eine aktuelle Problematik. Vor dem Hintergrund des vermehrten Zuzugs von Migrantinnen und Migranten aus südlichen Staaten – beispielsweise aus dem vom Bürgerkrieg betroffenen Syrien – nehmen in Deutschland die Prävalenzen von bestimmten hämatologischen Erkrankungen und Infektionskrankheiten zu. „Wir sehen eine Zunahme der hereditären hämatologischen Erkrankun-gen wie den hämolytischen Anämien, zu denen wir die Thalassämie oder die Sichelzellanämie zählen.“ Solche Phänomene, wie das vermehrte Auftreten von eher seltenen Erkrankungen im ärztlichen Behandlungsalltag, so Hochhaus weiter, sei bei der Ausbildung junger Ärztinnen und Ärzten zu berücksichtigen.
Die medikamentöse Versorgung: Schwächen im System
Dass es in der medikamentösen Therapie von hämatologischen Erkrankungen und soliden Tumoren trotz der großer Innovationen, der Verfügbarkeit vieler neuer Arzneimittel und der damit einhergehenden therapeutischen Erfolge verschiedene Probleme zu lösen gebe, machte Prof. Carsten Bokemeyer, Geschäftsführender Vorsitzender der DGHO und Direktor der II. Medizinischen Klinik und Poliklinik für den Bereich Onkologie, Hämatologie und Kno-chenmarktransplantation mit Sektion Pneumologie am Universitätsklinikum Hamburg-Eppendorf, deutlich. „Als Fachgesellschaft sehen wir derzeit verschiedene Problemfelder:
Vor dem Hintergrund der aktuellen Ausschreibungen für die Herstellung und Lieferung von Zytostatika durch von den Krankenkassen zentral ausgewählte Apotheken wies Bokemeyer auf die vielfältigen organisatorischen Probleme wie unterschiedliche Bestellsysteme, ver-schiedene Lieferzeiten und Applikationssysteme u. ä. hin. Dabei sei auch nicht klar, wie eine notwendige Qualitätskontrolle organisiert werden könne. „Die Zubereitung von Zytostatika ist komplex, die räumliche Nähe der Apotheken zu den Kliniken und Praxen ist wichtig, um eine schnelle und sichere Lieferung zu garantieren. Der Wunsch nach Kostenersparnis der Kran-kenkassen ist nachvollziehbar, aber diese Kostenersparnis darf nicht die Versorgungsqualität und die Patientensicherheit gefährden“, so Bokemeyer. Mit Blick auf die aktuell vom Gemeinsamen Bundesausschuss (G-BA) im Verfahren der Frühen Nutzenbewertung nach AMNOG bei bestimmten Arzneimitteln festgestellten Ergebnisse „kein Zusatznutzen belegt“ stellte Bokemeyer fest: „Der G-BA hat in den aktuellsten Verfahren mehrfach keinen Zusatznutzen festgestellt, obwohl die Arzneimittel zu einer Verlängerung der Überlebenszeit führen. Aus unserer Sicht besteht die Gefahr, dass es in Folge der Entscheidungen des G-BA auf Grundlage der Formel ‚Verlängerung der Überlebenszeit abzüglich Nebenwirklungen = Zusatznutzen nicht belegt‘ zu Fehlentwicklungen kommt und die Gefahr besteht, dass der Zugang zu neuen Arzneimitteln insbesondere für Krebspatienten in schwierigen oder fast aussichtslosen Situationen erschwert wird.“ Bei der Frühen Nutzenbewertung neuer Arzneimittel müssten Endpunkte wie Überlebenszeit gegenüber potenziellen und reversiblen Nebenwirkungen stärker gewichtet werden. Darüber hinaus, so der Geschäftsführende Vorsitzende, müssten der Fokus auf Patientengruppen mit ungedecktem medizinischem Bedarf gelegt werden. „Bei Vorliegen überzeugender Daten zum Ansprechen und zur Verträglichkeit in definierten Subgruppen sollte ein befristeter Zusatznutzen ausge-sprochen werden. Hier können uns unabhängige Register zusätzlich helfen, den Zusatznut-zen in der Versorgungsqualität zu quantifizieren.“ Hämatologie und Onkologie im Spannungsfeld der Ökonomie
Prof. Hellmut Samonigg, Präsident der Österreichischen Gesellschaft für Hämatologie und Medizinische Onkologie (OeGHO) wies auf die Herausforderungen der Behandlung von soli-den Tumoren und hämatologischen Erkrankungen für die Volkswirtschaften der Länder hin. „Durch die Erfolge in der medikamentösen Tumortherapie haben wir bestimmte Entitäten immer besser im Griff und beobachten chronische Verläufe, wo wir bislang nur kurze Überle-benszeiten sahen.“ Darüber hinaus trage der demografische Wandel dazu bei, dass immer mehr Patientinnen und Patienten behandelt werden müssten. „Das sind selbstverständlich alles Entwicklungen, über die wir in der medikamentösen Tumortherapie Tätigen äußerst froh sind. Klar ist aber auch, dass wir uns mit den daraus resultierenden steigenden Kosten für unsere Volkswirtschaften auseinandersetzen müssen.“ Quelle: Deutsche Gesellschaft f. Hämatologie und Onkologie (DGHO)
Stammzellforschung – Von der Krebsursache zum medizinischen Fortschritt
Zum nunmehr sechsten mal richtet das Deutsche Krebsforschungszentrum (DKFZ) vom 18. bis 20. September 2016 das Internationale Heinrich F.C. Behr-Symposium aus, dass alle zwei Jahre stattfindet. Rund 400 Experten aus aller Welt tauschen sich aus, um über Stammzellen, Krebs und Krebsstammzellen zu berichten und zu diskutieren.
“…Wir sind davon überzeugt, dass dieses Forschungsgebiet die Behandlung von Krebspatienten in Zukunft entscheidend beeinflussen und verbessern wird”, sagt Michael Boutros, der kommissarische Wissenschaftliche Vorstand des DKFZ. “Das zeigen allein schon einige der Ergebnisse, die auf dem diesjährigen Symposium vorgestellt werden.” “Die Krebsstammzellforschung ist in der Medizin angekommen”, freut sich Andreas Trumpp vom DKFZ und von HI-STEM, dem “Heidelberger Institut für Stammzellforschung und experimentelle Medizin, das das DKFZ mit der Dietmar Hopp Stiftung gegründet hat. “Die Aufklärung der Tricks der Krebsstammzellen liefert uns wertvolle Ideen für die Therapie, die wir nun beginnen umzusetzen. Und mit 3D-Kulturen von Tumoren können wir das Tumorgeschehen in der Petrischale nachahmen und gleichzeitig Strategien für die Behandlung entwickeln.”
Erblich bedingten Brustkrebs
Von der Stammzellforschung zur Brustkrebs-Prävention – das ist das Ziel von Jane Visvader vom Walter and Eliza Hall Institute in Melbourne, Australien. 2006 ist es ihr als erster gelungen, die Brustdrüsen-Stammzellen zu identifizieren. Nun hat sie herausgefunden, wie genetische Veränderungen bestimmte Tochterzellen dieser Stammzellen zu einer besonders gefährlichen Form von Brustkrebs entarten lassen, und wie man diesen Prozess mit einem Medikament verhindern kann. Dies könnte die Prävention von erblich bedingtem Brustkrebs erheblich verbessern, als Alternative zur bisher oft vorgenommenen Radikaloperation.
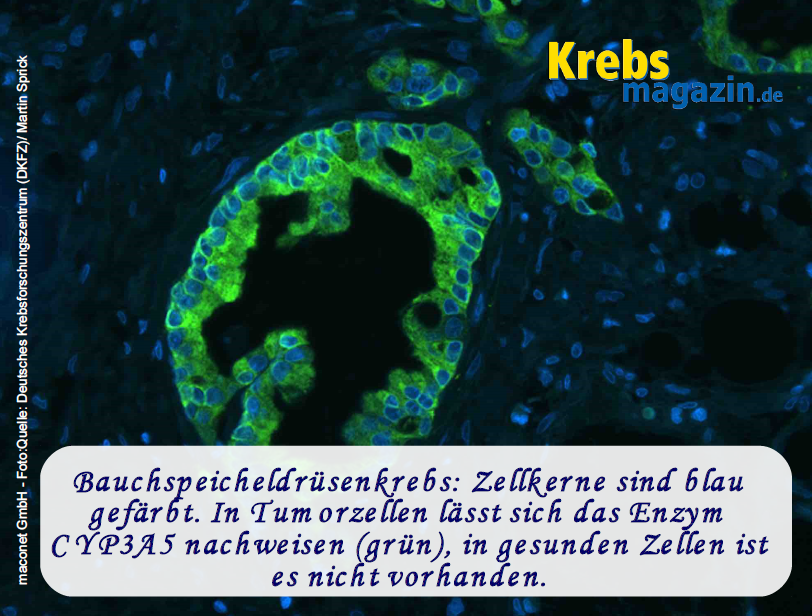
Bauchspeicheldrüsenkrebs
Andreas Trumpp berichtet darüber, wie verschiedene Krebsstammzellen unterschiedliche Typen von Bauchspeicheldrüsenkrebs hervorrufen. Auf der Basis dieser Forschung fand er heraus, warum einer der Subtypen von Bauchspeicheldrüsenkrebs so besonders resistent gegen Chemotherapien ist und wie sich hieraus ein neuer Ansatz ergeben könnte, um wirksamere Therapien zu entwickeln.
Organoide zum besseren Verständnis für Organentwicklung und Krankheitsentstehung
Ein besonders spannendes Thema der aktuellen Stammzellforschung sind so genannte Organoide, in der Kulturschale aus Stammzellen gezüchtete organähnliche Strukturen. Für die Grundlagenforschung haben sie großes Potential, um beispielsweise zu verstehen, wie sich Organe entwickeln oder wie Krankheiten entstehen. In der medizinischen Forschung verspricht man sich Fortschritte bei der Entwicklung von Organersatz, sie gelten außerdem als ideal, um neue Wirkstoffe zu erproben.
Gehirn in der Kulturschale
Jürgen Knoblich vom Institut für Molekulare Biotechnologie in Wien stellt das besonders aufsehenerregende und hochkomplexe menschliche “Gehirn in der Kulturschale” vor, das tatsächlich aus verschiedenen gehirntypischen Strukturen aufgebaut ist und aktive Nervenzellen enthält.
Organoide aus patienteneigenen Krebszellen zur zielgerichteten Therapie
Dem niederländischen Stammzellforscher Hans Clevers vom Hubrecht Institut für Entwicklungsbiologie und Stammzellforschung in Utrecht ist es erstmals gelungen, Organoide aus patienteneigenen Krebszellen zu züchten. An diesen Gewebestrukturen können die Wissenschaftler und Ärzte prüfen, welche zielgerichteten Medikamente oder Medikamentenkombinationen am wirksamsten sind und so die Therapie vorab an den individuellen Tumor anpassen.
Quelle: Deutsches Krebsforschungszentrum (DKFZ), Internationale Heinrich F.C. Behr-Symposium, 18. bis 20. September 2016
Den Menschen therapieren, nicht nur den Tumor – Lebensqualität steht bei Jahreskongress der Strahlentherapeuten im Fokus
Krebspatienten können durch ihre Erkrankung und deren Symptome schwer belastet sein. Doch auch die Therapie des Tumors kann sie zusätzlich beeinträchtigen: Operation, Chemotherapie und Bestrahlung können Nebenwirkungen und Spätfolgen haben, die die Lebensqualität der Betroffenen einschränken. „Der gesundheitliche Preis, den Patienten für Heilung oder Lebensverlängerung zahlen müssen, ist in den vergangenen zwanzig Jahren immer stärker in den Fokus der Medizin gerückt“, sagt Tagungspräsident Professor Dr. med. Frederik Wenz. Auf der 22. Jahrestagung der Deutschen Gesellschaft für Radioonkologie (DEGRO) vom 16. bis 19. Juni 2016 in Mannheim wird die Lebensqualität der Patienten nun ein Schwerpunktthema sein.
Die Experten der DEGRO stellen auf ihrer Jahrestagung in Mannheim neue Bestrahlungstechniken und Begleitbehandlungen vor, die zum Erhalt oder zur Verbesserung der Lebensqualität beitragen. „Lebensqualität ist ein ganzheitlicher Begriff, der nicht nur körperliche Aspekte umfasst, sondern auch psychische und soziale“, sagt Professor Dr. med. Dirk Vordermark, Direktor der Klinik für Strahlentherapie am Universitätsklinikum Halle (Saale) und Sprecher der DEGRO-Arbeitsgruppe „Lebensqualität und Ethik in der Radioonkologie“.
Ärzte können die Lebensqualität ihrer Patienten jedoch oft nicht richtig einschätzen. So empfinden einige Patienten diese selbst in der Endphase einer unheilbaren Krebserkrankung als gut. Andere, die ihren Krebs bereits überwunden haben und als geheilt gelten, leiden hingegen unter starken Belastungen und Einschränkungen. Als Beispiel nennt Vordermark die Therapie von Prostatatumoren, die oft Inkontinenz oder Impotenz nach sich ziehen kann, oder Sprech- und Schluckstörungen, die durch die Behandlung von Tumoren im Halsbereich entstehen können.
„Lebensqualität ist immer subjektiv“, sagt Dirk Vordermark. „Die Schwierigkeit besteht darin, sie zu objektivieren und messbar zu machen.“ Eine Möglichkeit hierfür bieten standardisierte und auf die jeweilige Krebsart abgestimmte Fragebögen, die von der Quality of Life Group der European Organization for Research and Treatment of Cancer (EORTC) entwickelt wurden.
Mithilfe der Fragebögen schätzen die Patienten selbst ihre Lebensqualität ein. Das Ergebnis ist ein Zahlenwert, der Vergleiche erlaubt. „Wenn die Patienten vor, während und nach der Behandlung befragt werden, können so die Auswirkungen der Therapie auf die Lebensqualität untersucht werden“, erläutert Vordermark. Das sei sowohl bei heilenden, als auch bei palliativen, also lindernden Therapieansätzen wichtig. Ist das Ziel die Heilung, werden kurzfristig auch stärkere Nebenwirkungen in Kauf genommen. Langfristig soll der Patient aber so wenige Einschränkungen wie möglich davontragen. Wird die Strahlentherapie jedoch palliativ eingesetzt, soll sie dazu beitragen, die Lebensqualität rasch zu stabilisieren oder gar zu verbessern.
Wie weit die Lebensqualität des einzelnen Patienten im Klinikalltag mithilfe von Fragebögen erfasst werden kann, wird derzeit in Pilotstudien geprüft. „Solche Rückmeldungen einzuholen ist sehr aufwendig, aber lohnenswert“, sagt Tagungspräsident Wenz, der die Klinik für Strahlentherapie und Radioonkologie am Universitätsklinikum Mannheim leitet. Denn wenn der Tumor zwar kleiner werde, es dem Patienten aber subjektiv schlechter gehe, sei nicht viel gewonnen.
Die technischen Fortschritte in der Strahlentherapie ermöglichen es heute, den Tumor gezielt zu bestrahlen und zugleich das gesunde Gewebe zu schonen. „Wir haben bereits viel darüber gelernt, welche Therapiekonzepte und welche Strahlendosis zu einer möglichst guten Lebensqualität führen“, erklärt der DEGRO-Experte. „Allerdings müssen wir dieses Wissen weiter ausbauen, sodass die Patienten noch mehr davon profitieren.“
Quelle: DEGRO – Deutschen Gesellschaft für Radioonkologie e.V.
DKK 2016: Verdrängungswettbewerb zu Lasten der Patienten
Der Berufsverband der Hämatologen und Onkologen (BNHO) weist erneut darauf hin, dass durch die zunehmende wettbewerbliche Orientierung der Leistungsanbieter sich immer mehr Onkologen im Spannungsfeld zwischen ärztlichem Selbstverständnis und harten wirtschaftlichen Zwängen befinden. Krebspatienten erwarten von ihren behandelnden Ärzten zurecht, dass therapeutische Entscheidungen nicht von ökonomischen Interessen beeinflusst werden. Um die patientenorientierte onkologische Versorgung in Deutschland zu erhalten, dürfen Kostendiskussionen ärztliches Handeln nicht überlagern. Und es müssen patientenorientierte – und nicht marktorientierte – Rahmenbedingungen geschaffen werden.
 Prof. Dr. Stephan Schmitz, Onkologe, Köln
Prof. Dr. Stephan Schmitz, Onkologe, Köln
“Der Krebspatient möchte nicht Teil einer Wertschöpfungskette sein. Er erwartet vielmehr eine Versorgung, die sowohl seine qualitativen als auch seine emotionalen und sozialen Ansprüche vollumfänglich erfüllt”, betonte der Vorsitzende des Berufsverbands der Niedergelassenen Hämatologen und Onkologen in Deutschland – BNHO e.V., Prof. Stephan Schmitz, beim 32. Deutschen Krebskongress in Berlin. Zu einer patientenorientierten Versorgung gehören Schmitz zufolge höchste fachliche Kompetenz, aber auch die Bereitschaft, sich für die Patienten Zeit zu nehmen, ihnen über teilweise viele Jahre als konstanter Ansprechpartner zur Verfügung zu stehen und die oft komplexe onkologische Versorgung über die reine onkologische Therapie hinaus zu koordinieren.
Bei einem BNHO-Symposium im Rahmen des Deutschen Krebskongresses diskutierten Onkologen, Versorgungsforscher und Medizinethiker, inwieweit die derzeit im deutschen Gesundheitswesen zu beobachtenden strukturellen Veränderungen die Ansprüche an eine patientenorientierte Versorgung auf Dauer erfüllen können. Bisher wird ein erheblicher Teil der onkologischen Patienten, über 600.000 pro Jahr, wohnortnah in hämatologisch-onkologischen Schwerpunktpraxen versorgt. Seit einigen Jahren drängen aber auch die Krankenhäuser verstärkt in die ambulante onkologische Versorgung. “Das führt leider vielerorts nicht zu einem Wettbewerb um mehr Qualität, sondern zu profitorientierten Versorgungsstrukturen, bei denen der Patient nur eine Nebenrolle einnimmt”, so Schmitz.
Klare Wettbewerbsnachteile für freiberufliche Krebsspezialisten
Ein Kernproblem dabei ist, dass die gesundheitspolitischen Rahmenbedingungen einen fairen Wettbewerb zwischen freiberuflichem Onkologen und Krankenhaus verhindern. Deutlich wird das in einer neuen, vom BNHO beauftragten Studie zur wettbewerblichen Analyse der ambulanten onkologischen Versorgung. Studienleiter Prof. Justus Haucap stellte die wichtigsten Ergebnisse dieser Untersuchung in Berlin vor. Demnach hätten die freiberuflichen, niedergelassenen Onkologen im derzeitigen Versorgungssystem ganz erhebliche Wettbewerbsnachteile im Vergleich zu den Krankenhäusern.
Warnung vor immer stärkerer Industrialisierung der Versorgung
Auf den mittlerweile unübersehbaren Trend zu einer Mengenausweitung weist seit Jahren der Medizinethiker Prof. Giovanni Maio aus Freiburg hin. Beim BNHO-Symposium in Berlin warnte er vor eine Industrialisierung der Krankenversorgung, bei der die eigentliche Leistung des Arztes nicht abgebildet werde und der Patient daher als Person vor lauter diagnostischem und therapeutischem Aktionismus aus dem Blick gerät.
Mittelständisch geprägte Versorgungsstrukturen mit niedergelassenen Fachärzten, die nah am Alltag der Patienten sind, wirken einer Industrialisierung der Medizin entgegen, betonte Dr. Walter Baumann vom Wissenschaftlichen Institut der Niedergelassenen Hämatologen und Onkologen (WINHO) in Köln. Es müssten tragfähige Kooperationsstrukturen geschaffen werden, die ein faires Nebeneinander der Versorgungsebenen ermöglichen, statt einem Verdrängungswettbewerb und einer lokalen Monopolbildung Vorschub zu leisten, die letztlich zulasten des Patienten gehe.
Quelle: BNHO Berufsverband der niedergelassenen Hämatologen und Onkologen in Deutschland
DKK 2016 – Krankheitsbewältigung: Neue Patientenleitlinie zur Psychoonkologie
Der Bundesverband Prostatakrebs Selbsthilfe e.V. (BPS) weist auf eine neue Behandlungsleitlinie zur Psychoonkologie hin, die von der Stiftung Deutsche Krebshilfe und medizinischen Fachgesellschaften gemeinsam mit Patientenvertretern entwickelt wurde.
Download der Patientenleitlinie
Im Rahmen des laufenden 32. Deutschen Krebskongresses in Berlin ist die neue Patienten-Leitlinie „Psychoonkologie – Psychosoziale Unterstützung für Krebspatienten und Angehörige“ erschienen. Die Empfehlung beruht auf der bereits bestehenden Handlungsempfehlung der ärztlichen S3-Leitlinie “Psychoonkologische Diagnostik, Beratung und Behandlung von erwachsenen Krebspatienten” des Leitlinienprogramms Onkologie und damit auf dem besten derzeit verfügbaren medizinischen Wissen. „In dem Zusammenhang wünschen wir uns sehr, dass die Ärzte die neue Empfehlung umsetzen“, so Joachim Böckmann, Vorstandsmitglied des Bundesverbandes Prostatakrebs Selbsthilfe e.V. (BPS) und Vorsitzender des BPS-Arbeitskreises „Psychoonkologie“ am Freitag in Berlin.
Die Diagnose Krebs verändert das Leben von Patienten und deren Angehörigen. Oftmals sind nicht körperliche sondern seelische und soziale Belastungen die Folge. Hier setzt die Psychoonkologie an, sie hilft Patienten, mit den vielfältigen Veränderungen besser umgehen zu können.
Eine weitere Besonderheit? Die Patientenbroschüre ist in einer laienverständlichen Sprache geschrieben. „Dies ist äußerst wichtig für Patienten und Angehörige. Fachbegriffe sind bei Medizinern an der Tagesordnung, führen aber oft zur Verunsicherung bei Patienten. Dies ist nun vorüber“, so Böckmann weiter. Die neue Patienten-Leitlinie wurde von der Stiftung Deutsche Krebshilfe (DKH), der Deutschen Krebsgesellschaft (DKG) und von den Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) finanziert und gemeinsam mit Patientenvertretern in den vergangenen zwei Jahren entwickelt. Der BPS war an der Erarbeitung intensiv beteiligt. „Wir sind mit dem Ergebnis sehr zufrieden.
Gerade viele Männer tun sich mit ihrer Psyche recht schwer! Diese Leitlinie hilft, Ängste und bekannte Zurückhaltung der Männer ein wenig zu überwinden“, so BPS-Vertreter und Mitglied der Arbeitsgruppe Berthold Isele. Ursula Reitberger vom BPS-Arbeitskreis „Frauen“ kommentierte vergangenes Jahr die Konsultationsfassung, sie wünscht sich: „Die Bedeutung der Psychoonkologie sollte an Wert gewinnen, sowohl in der Öffentlichkeit, als auch innerhalb der Ärzteschaft. Es wäre schön, wenn die neue Patientenversion dazu beitragen könnte.“
Quelle: Bundesverband Prostatakrebs Selbsthilfe e.V. – BPS
DKK 2016: Niedergelassene Hämatologen und Onkologen warnen vor “Rationierung durch die Hintertür”
Der Berufsverband warnt vor einem Angriff auf die Therapiefreiheit zu Lasten der Krebspatienten
Bei der medikamentösen Versorgung von Krebspatienten in Deutschland wird seit Neuestem versucht, wirksame Therapien gezielt von der Erstattung durch die Gesetzliche Krankenversicherung auszunehmen. Anlässlich des Deutschen Krebskongresses warnt der Berufsverband der Niedergelassenen Hämatologen und Onkologen in Deutschland – BNHO e. V. vor dieser „Rationierung durch die Hintertür“.
Mit dem so genannten AMNOG-Verfahren wurde in Deutschland vor fünf Jahren ein neues Bewertungsverfahren für innovative Arzneimittel eingeführt, bei dem nach der arzneimittelrechtlichen Zulassung der Patientennutzen im Rahmen einer „frühen Nutzenbewertung“ noch einmal separat abgeschätzt wird. Das Ergebnis der frühen Nutzenbewertung bildet die Grundlage für Preisverhandlungen bzw. Rabattverträge zwischen den pharmazeutischen Unternehmen und den Krankenkassen: Je höher der Zusatznutzen, umso besser ist der Preis, den der Hersteller für sein Medikament im
GKV-System erzielen kann. So weit, so fair. „Mittlerweile ist aber zu beobachten, dass das als Instrument der Preisfindung zwischen Industrie und GKV entwickelte AMNOG-Verfahren dafür missbraucht wird, die Erstattung wirksamer Medikamente bei Krebspatienten einzuschränken und damit in die Therapiefreiheit des Arztes fundamental und unzulässig einzugreifen“, betonte der BNHO-Vorsitzende Prof. Dr. Stephan Schmitz. Hoch wirksame Krebsmedikamente sollen nur noch Krebspatienten zu Lasten der GKV verordnet werden dürfen, bei denen das AMNOG-Verfahren einen Zusatznutzen gegenüber (kostengünstigeren) Vergleichstherapien bescheinigt hat. Damit wäre ein
Medikament ohne Zusatznutzen bei Patienten trotz nachgewiesener Wirksamkeit nicht verordnungsfähig.
Konkret enthält beispielsweise die Arzneimittelvereinbarung zwischen der KV Bayern und bayerischen Krankenkassen einen Passus, wonach „Arzneimittel, bei denen der Gemeinsame Bundesausschuss einen Zusatznutzen festgestellt hat, […] grundsätzlich nur in den Anwendungsgebieten mit Zusatznutzen verordnet“ werden sollen. „Damit wird versucht, in die Therapiekompetenz des Arztes einzugreifen und aus Kostengründen unter dem Mantel einer ‚wirtschaftlichen Verordnung’ Krebspatienten wirksame Medikamente vorzuenthalten. Hier liegt ganz klar eine nicht zulässige Rationierung vor, die die Versorgung verschlechtern und letztlich Leben kosten kann“, betonte Dr. Robert Dengler, der die bayerischen Verhältnisse als Geschäftsführer des BNHO Bayern und aus seiner hämatologisch-onkologischen Schwerpunktpraxis in Regensburg aus erster Hand kennt.
Der BNHO möchte den Deutschen Krebskongress 2016 nutzen, um mit Nachdruck vor dieser gefährlichen Entwicklung zu warnen. Bei einem Kongresssymposium unter dem gemeinsamen Vorsitz des BNHO und der Deutschen Krebsgesellschaft wurde das Thema unter anderem mit Vertretern der Kassenärztlichen Vereinigung Bayerns und auch der Kostenträger diskutiert. „Es gab Anfang des Jahrtausends im Zusammenhang mit dem Off-Label-Use schon einmal den Versuch, die Verordnung wirksamer Medikamente einzuschränken. Das ist damals zurecht gescheitert. Wir müssen das jetzt
nicht unter anderen Vorzeichen wiederholen“, so Schmitz.
Für die Kassenärztliche Vereinigung Bayerns betonte Johann Fischaleck, dass das AMONG weder den Stellenwert neuer Arzneimittel innerhalb des medizinischen Standards noch innerhalb der Leitlinien festlege: „Dies müssen die Fachgesellschaften leisten“, so Fischaleck. Seien zwei Interventionen medizinisch vergleichbar, müsse allerdings die kostengünstigere eingesetzt werden.
Der BNHO schließt sich dieser Auffassung im Prinzip an, verwahrt sich aber dagegen, dass Medikamente nur wegen eines nicht nachgewiesenen Zusatznutzens aus der Erstattung genommen werden. Auch ohne Nachweis eines Zusatznutzens handelt es sich um hoch wirksame, arzneimittelrechtlich zugelassene Medikamente. „Gerade bei fortgeschrittenen Krebserkrankungen ist es häufig notwendig, dass es verschiedene wirksame Medikamente für die Patienten gibt, die in Kombination oder sequenziell eingesetzt werden können. Nur so erreiche man eine lange Tumorrückbildung (Remission). Krebsmedikamente wirken am Anfang häufig sehr gut, dann entwickeln sich aber Resistenzen, und man braucht ein weiteres Medikament – ein wirksames Medikament und nicht nur ein Medikament, das im AMNOG-Verfahren einen Zusatznutzen gezeigt hat“, betonte Schmitz. „Die Entscheidung über diese patientenindividuelle Therapie muss auch in Zukunft allein beim Arzt liegen.“
Quelle: Berufsverband der Niedergelassenen Hämatologen und Onkologen in Deutschland – BNHO e.V.
Moderne Krebsmedizin: präventiv, personalisiert, präzise und partizipativ
Die Chancen moderner Krebsmedizin: innovative Therapien für den individuellen Patienten
Anhand der Forschungsergebnisse der Wissenschaftler um Professor Dr. Matthias Fischer von der Universitätskinderklinik zu Köln wird deutlich, wie wichtig die genaue molekulare Charakterisierung von Tumoren für die Entwicklung verbesserter Therapien ist. Der Mediziner untersucht genetische Veränderungen im Neuroblastom, das zu den häufigsten Tumorarten im Kindesalter gehört. In manchen Fällen bildet sich das Neuroblastom ohne jegliche Therapie komplett zurück, bei anderen Patienten jedoch schreitet es trotz Therapie unaufhaltsam voran. Die Gründe dafür waren bisher weitgehend unbekannt. Die Kölner Wissenschaftler konnten nun die genetischen Veränderungen, die zu einem aggressiven Krankheitsverlauf führen, identifizieren. „Unsere Erkenntnisse verändern unser Verständnis der Entwicklung des Neuroblastoms fundamental und könnten in Zukunft Diagnostik und Therapie des Neuroblastoms maßgeblich beeinflussen“, so Professor Fischer.
Dr. Fritz Pleitgen, Präsident der Deutschen Krebshilfe, hält es für wichtig, bei allen Diskussionen zu den verschiedenen Themenkomplexen des Kongresses immer die Patientenbelange im Blick zu haben. Dabei dürfe auch der zwischenmenschliche Aspekt der Krebsmedizin nicht vernachlässigt werden. „Der Krebspatient von heute möchte als aktiver, gleichberechtigter Partner angesprochen werden. Die traditionell geprägte Arzt-Patient-Beziehung ist ein Auslaufmodell – der paternalistisch handelnde Arzt hält den heutigen Herausforderungen nicht mehr stand. Die Patienten wollen aktiv zu einer Verbesserung des Krankheitsverlaufes beitragen und mitentscheiden.“ Hierbei gelte es insbesondere, die kommunikativen Kompetenzen von Ärzten und anderen Heilberuflern zu verbessern sowie die Gesundheitskompetenz der Allgemeinbevölkerung und insbesondere der Krebspatienten zu stärken.
Genetisches Profiling – In der Krebsmedizin ist die genetische Diagnostik mittlerweile unverzichtbar
Anlässlich des 32. Deutschen Krebskongresses 2016 in dessen Rahmen am 27. Februar auch der Krebsaktionstag für Laien und Betroffene angeboten wird, hat die Deutsche Krebsgesellschaft e.V. und die Deutsche Krebshilfe gemeinsam mit der Berliner Krebsgesellschaft drei Referenten interviewt, die wir hier ungekürzt veröffentlichen möchten.
Noch vor wenigen Jahren war die DNA-Sequenzierung ausschließlich ein Werkzeug der Grundlagenforscher zur Entschlüsselung des genetischen Codes. Mittlerweile hat diese Technik Einzug in die Klinik gehalten. Denn Genmutationen, die man im Tumor findet, können wertvolle Informationen für die gezielte Therapieauswahl liefern.
Prof. Dr. Christoph Röcken, Sprecher der Arbeitsgemeinschaft Onkologische Pathologie in der Deutschen Krebsgesellschaft, erklärt im Interview, wie ein genetisches Tumorprofil erstellt wird und beschreibt die Herausforderungen.
Herr Professor Röcken, können Sie Beispiele nennen, wo eine Genveränderung im Erbgut des Tumors heute schon den Weg zur gezielten Therapie weist?
Das gilt mittlerweile beim Dickdarmkrebs, beim Lungenkrebs, beim schwarzen Hautkrebs, bei Hirntumoren und seit 2015 auch beim Eierstockkrebs. Bei diesen Krebsarten erhalten Pathologen häufig den Auftrag, herauszufinden, ob der Tumor bestimmte Mutationen trägt.
Wie wird das Ausgangsmaterial für die Analyse gewonnen?
Wir starten mit Biopsiematerial oder mit Tumorgewebe aus einer OP und fertigen daraus zunächst Gewebeschnitte an. Anschließend grenzen wir unter dem Mikroskop das Tumorareal ein und berücksichtigen dabei die Heterogenität des Tumors. Die fraglichen Areale werden gezielt herauspräpariert (mikrodisseziert), man gewinnt daraus die DNA und untersucht sie anschließend mit einer DNA-Sequenzierung auf Mutationen.
Welche Sequenzierungsmethoden kommen dabei zum Einsatz?
In der diagnostischen Routine geht es häufig um die Frage, ob ein bestimmtes Gen eine bestimmte Mutation trägt. D.h. der entsprechende Gen-Abschnitt wird zunächst vervielfältigt und dann einer klassischen Sanger-Sequenzierung unterzogen. Mittlerweile sind aber viele Gene bekannt, die in der Diagnostik und Therapie eine Bedeutung haben. Will man die alle mit der klassischen Methode überprüfen, muss man jedes Gen einzeln sequenzieren – ein enormer Zeitaufwand. Das Next Generation Sequencing, kurz NGS, erlaubt die parallele Sequenzierung vieler Gene. Damit lassen sich z. B. 10 bis 40 Gene auf einmal untersuchen, und zwar in einer sogenannten Panel-Sequenzierung. Das steigert die Effizienz der Sequenzierung enorm.
Mit sogenannten Liquid Biopsies wollen die Experten mittlerweile auch im Blut nach der mutierten Krebs-DNA suchen. Wie zuverlässig ist diese Diagnostik?
Dass Tumor-DNA oder auch Tumorzellen im Blut vorkommen, weiß man schon länger. Hämatologen nutzen das bei bestimmten Leukämien, und zwar zur Bestimmung der Resterkrankung nach der Therapie. Diese Leukämien tragen eine charakteristische Mutation; je geringer die Konzentration an mutierter DNA im Blut, desto geringer die minimale Resterkrankung. Auch solide Tumoren können beim Untergang von Tumorzellen DNA ins Blut freisetzen. Das gilt allerdings nicht für alle Tumorarten in jedem Tumorstadium. Annähernd 100% der Patienten mit fortgeschrittenem Darmkrebs weisen zirkulierende Tumor-DNA im Blut auf, nur 40% beim Prostata- oder Nierenkarzinom, und beim Hirntumor findet man gar keine Tumor-DNA im Blut.
Gibt es noch weitere Einschränkungen?
Man muss die Mutation, nach der gesucht werden soll, genau kennen. Eine Liquid Biopsy zur Suche nach einer Genveränderung, die der Tumor gar nicht trägt, macht keinen Sinn. An der Erstellung eines genetischen Profils des Tumors kommt man also nicht vorbei. Außerdem kommen einige der Mutationen, die wir in bösartigen Tumoren finden, auch bei gutartigen Tumoren vor. Insgesamt ist also noch einiges an Standardisierung und Qualitätssicherung nötig, bevor die Liquid Biopsy bei Patienten mit soliden Tumoren routinemäßig angewendet werden kann. Zur Überprüfung des Therapieansprechens bei Patienten mit einer hohen Tumorlast könnten Liquid Biopsies aber durchaus nützlich sein.
Was verändert sich durch die genetische Diagnostik in der Pathologie?
Für die Einteilung von Tumoren ist sie mittlerweile unverzichtbar und ich sehe darin eine große Chance, um die Therapie noch genauer auf die Biologie des Tumors abstimmen zu können. Natürlich unterliegt diese Art der Diagnostik einer großen Dynamik, und wir sind gefordert, mit dem raschen Zuwachs an Wissen und der Entwicklung neuer Methoden Schritt zu halten. Deshalb sind Kongresse wie der DKK 2016 wichtig, bei dem die Experten zusammenkommen, um ihr Wissen auszutauschen. Vor allem im translationalen Programmteil des DKK 2016 sind die Themen Molecular Diagnostics, Next Generation Sequencing und Liquid Biopsy vertreten. Ich verspreche mir interessante Beiträge und spannende Sitzungen vom DKK 2016.
Quelle: Deutsche Krebsgesellschaft, Deutsche Krebshilfe