Archiv für die Kategorie „Brustkrebs“
Molekulardiagnostik in der Krebsmedizin
Die Diagnostik und Therapie maligner Erkrankungen befinden sich in einem tiefgreifenden Wandel. Krebs spaltet sich zunehmend in eine Vielzahl verschiedener Erkrankungen auf, jede mit ganz einzigartigen Merkmalen. Grundlage jeder therapeutischen Maßnahme ist eine differenzierte Diagnostik. Eine zunehmende Rolle spielt in diesem Zusammenhang die Molekulardiagnostik. Ihre Möglichkeiten sind vielfältig, die Analysen komplex, die Erwartungen sehr hoch. Angesichts der Vielfalt der Möglichkeiten und der dynamischen Entwicklung in der Onkologie hat die DGHO Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie e. V. in Kooperation mit weiteren wissenschaftlichen medizinischen Fachgesellschaften ein gemeinsames Positionspapier erarbeitet, das den Einsatz der Molekulardiagnostik in der Versorgung von Patientinnen und Patienten mit Krebs definiert. Gemeinsam mit der Deutschen Krebsgesellschaft und der Deutschen Gesellschaft für Pathologie hat die DGHO das Positionspapier in Berlin vorgestellt.
Indikationsfelder und Beispiele
Prof. Dr. med. Olaf Ortmann, Präsident der Deutschen Krebsgesellschaft (DKG) und Direktor der Klinik für Frauenheilkunde und Geburtshilfe am Caritas-Krankenhaus St. Josef in Regensburg sowie Inhaber des Lehrstuhls für Frauenheilkunde und Geburtshilfe an der Universität Regensburg, machte die Relevanz der stetigen Zunahme der Zahl von molekulardiagnostisch nachgewiesenen, krankheitsbezogenen “Abweichungen von der Norm durch Chromosomenänderung” (Aberrationen) deutlich. “Für den Bereich der Früherkennung und Prävention gilt das beispielsweise für Keimbahnmutationen in den BRCA1- oder BRCA2-Genen, die wir als Risikofaktoren für ein Mamma- oder Ovarialkarzinom kennen. Dabei erlaubt uns der Nachweis und die Charakterisierung krankheitsspezifischer oder -assoziierter Aberrationen eine individuelle Risikoabschätzung und stellt die Basis weiterführender Empfehlungen bzw. Maßnahmen dar.” Im Bereich der Diagnose sind laut Ortmann molekulardiagnostische Verfahren zur Typisierung einer Tumorerkrankung dann indiziert, wenn mit konventionellen gewebediagnostischen Verfahren (zytologische oder histologische, mikroskopische Analysen) keine ausreichende Diagnosesicherung möglich ist, und wenn eine hinreichende Wahrscheinlichkeit besteht, mittels der ergänzenden (molekulargenetischen) Diagnostik eben diese Sicherheit zu erlangen.
Im Bereich der Therapie sind molekulardiagnostische Verfahren dann indiziert, wenn das Ergebnis vorhersagbare (prädiktive) Bedeutung hat, also den Nutzen einer möglichen Therapie vorhersagen kann. Als Beispiel nannte Ortmann das Mammakarzinom: “Mit der Publikation der TAILORx-Studie liegen jetzt erstmals Daten einer großen, prospektiv randomisierten Studie zum prädiktiven Wert einer Genexpressionsanalyse bei Patientinnen mit HR-positivem, nodal negativem Mammakarzinom vor. Auf Basis der TAILORx-Studie kann bei einer definierten Gruppe von Patientinnen mit Hormonrezeptor (HR)-positivem Mammakarzinom die Empfehlung zur adjuvanten Chemotherapie unterstützt, bei einer anderen Gruppe auf die Chemotherapie verzichtet werden”, so der Präsident der DKG.
Durchführung: Klinische Indikation, Ablauf und Interpretation der Ergebnisse
Prof. Dr. med. Carsten Bokemeyer, Vorsitzender der DGHO und Direktor der II. Medizinischen Klinik und Poliklinik für den Bereich Onkologie, Hämatologie und Knochenmarktransplantation mit Sektion Pneumologie am Universitätsklinikum Hamburg-Eppendorf, betonte, dass bei soliden Tumoren und auch bei vielen hämatologischen Neoplasien die Integration der Molekulardiagnostik in den Diagnose-Algorithmus die Auswahl des für den individuellen Patienten besten Therapiekonzeptes erst ermöglicht. Daher muss die molekulare Diagnostik im klinischen Kontext sinnvoll indiziert und interpretiert werden. “Am Ende der Diagnostik steht die interdisziplinäre Diskussion im Tumorboard (Tumorkonferenz) zur Erstellung der Therapieempfehlung für unsere Patientinnen und Patienten. An vielen Zentren sind in den letzten Jahren zudem molekulare Tumorboards mit besonderer Expertise in der Interpretation molekulardiagnostischer Befunde entstanden, die auch überregional zusammenarbeiten”, so Bokemeyer.
Wissen-generierende Versorgung
Durch die Fortschritte der Molekulardiagnostik hat sich die Erkenntnis verstärkt, dass Krebs nicht mehr als eine Krankheit, sondern vielmehr als Sammelbegriff für eine Vielzahl verschiedener Erkrankungen verstanden werden muss, so der Vorsitzende der DGHO. Dabei spaltet sich Krebs zunehmend in eine Vielzahl verschiedener Erkrankungen auf, jede mit definierten, zum Teil einzigartigen Merkmalen. Die mikroskopische Charakterisierung bösartiger Erkrankungen wurde ergänzt um eine komplexe biologische Diagnostik unter Verwendung molekulargenetischer und anderer Verfahren. Das führt vor allem zu einem grundsätzlichen Wandel der Therapie-Algorithmen. Diese Entwicklung ist noch längst nicht abgeschlossen, und die zukünftige Klassifikation von Erkrankungen mit den dazugehörigen Therapieempfehlungen wird auf den Erkenntnissen mit den jetzigen Instrumenten aufbauen. Darüber hinaus muss das individuell gewonnene Wissen aus der Diagnostik und Therapie der Patienten auch der medizinischen Entwicklung in unserer Gesellschaft im Sinne eines aus der Versorgung lernenden Systems zugutekommen. “Auch vor Ort in den jeweiligen Zentren ist ein kontinuierlicher Wissensaustausch zwischen den Diagnostikern und den Therapeuten unerlässlich. Das diagnostische Angebot muss ständig den sich rasch ändernden Anforderungen angepasst werden, zum Beispiel bei der Publikation Therapiestandard-verändernder Studiendaten oder beim Auftreten von Resistenzen unter Therapie mit gezielten Kinase-Inhibitoren”, so Bokemeyer.
Molekulare Testung: Methoden, Qualitätssicherung und die Rolle kommerzieller Anbieter
Prof. Dr. med. Wilko Weichert, Mitglied im Vorstand der Deutschen Gesellschaft für Pathologie (DGP) und Direktor des Instituts für Allgemeine Pathologie und Pathologische Anatomie der Technischen Universität München, verdeutlichte die rasante Entwicklung der molekulargenetischen Untersuchungstechniken in den letzten Jahren – von konventionellen Polymerasekettenreaktionen (PCR) oder Fluoreszenz-In-Situ-Hybridisierung (FISH) bis hin zum Next Generation Sequencing (NGS) mit Analyse des gesamten Exoms (Whole-Exome, WES), des gesamten Genoms (WGS) und des Transkriptoms (RNA-seq). Eine technische Herausforderung ist insbesondere die Analyse der meist kleinen, formalinfixierten, paraffineingebetteten Biopsiepartikel bei fortgeschrittenen Tumorerkrankungen, die einer Operation nicht mehr zugänglich sind. Bezüglich der genannten molekularen Charakterisierungen ist es zum jetzigen Zeitpunkt nicht sinnvoll, eine bestimmte Methode vorzugeben, vielmehr ist das Erreichen eines validen Ergebnisses in der jeweiligen Testung entscheidend. “Erforderlich ist die regelmäßige Durchführung der spezifischen molekulardiagnostischen Analysen und damit eine hohe technische Expertise, die externe Validierung der Analysequalität durch Teilnahme an Qualitätskontrollen in Form von Ringversuchen und eine Akkreditierung beziehungsweise Zertifizierung der Labore”, so Weichert. Dies kann dazu führen, dass nicht jedes Institut für Pathologie und nicht jedes hämatologische Labor eine umfassende Molekulardiagnostik anbieten kann. Aus diesem Grund ist der Auf- und Ausbau kooperativer Strukturen erforderlich, um den Arbeitsablauf und die Einhaltung der Kriterien der Qualitätssicherung zu garantieren.
In diesem Zusammenhang wies das Vorstandsmitglied der DGP auf die etwas kontrovers zu diskutierende Rolle von kommerziellen Anbietern hin, die zurzeit in einigen Bereichen versuchen, Elemente und Strukturen der molekularpathologischen Diagnostik in zentralisierter Form mit einem Fokus auf ökonomische Aspekte zu übernehmen. “Voraussetzung für jedwede Art kommerziell orientierter Molekulardiagnostik ist ihre Integration in den im Positionspapier skizzierten Arbeitsablauf. Dieser beginnt mit der gezielten Indikationsstellung, reicht über die sichere mikroskopische Identifikation von Tumorgewebe und die zielgerichtete Auswahl des korrekten Untersuchungsverfahrens über die qualifizierte Analyse einschließlich der Teilnahme an Qualitätssicherungsmaßnahmen bis zur umfassenden Diskussion der Ergebnisse im Tumorboard. Besonders wichtig erscheint in diesem Zusammenhang auch die volle Integration dieser Diagnostik in lokale beziehungsweise regionale klinisch-onkologische Strukturen, um den integralen Aspekt molekularer Diagnostik im Gesamtkontext der Behandlung nicht zu gefährden”, so Weichert.
Gesundheitspolitische Handlungsfelder
Anhand der Analyse des Ist- und Soll-Zustandes molekularer Diagnostik in der Onkologie sowie angesichts der Fülle diagnostischer und therapeutischer Innovationen ergibt sich auf verschiedenen Ebenen der Gesundheitspolitik Handlungsbedarf. “Wir müssen neben der Sicherstellung der flächendeckenden Verfügbarkeit der molekularen Diagnostik in der Onkologie und der Finanzierung auch die zeitnahe, qualitätsgesicherte Durchführung und die kontinuierliche ärztliche Fortbildung in der Molekulardiagnostik maligner Erkrankungen gewährleisten”, so Prof. Dr. med. Bernhard Wörmann, Medizinischer Leiter der DGHO. Darüber hinaus muss laut Wörmann durch eine kontinuierliche Analyse der Kosten molekularer Diagnostik im ambulanten und stationären Bereich eine Anpassung der Erstattung möglich sein. Außerdem ist die verbindliche Interpretation des Gendiagnostikgesetzes zur Analyse von genetischen Aberrationen notwendig, die gleichzeitig prädiktiv für die individuelle Tumortherapie sind, aber auch Hinweis auf eine hereditäre Belastung für die betroffenen Patientinnen und Patienten und ihre Angehörigen geben können. Des Weiteren gilt es, vor dem Hintergrund einer Patienten-orientierten Abwägung Angebote externer kommerzieller Anbieter gegenüber der Durchführung von Analysen im regionalen/nationalen Rahmen kritisch zu prüfen. “Dazu gehört für uns die Förderung des Aufbaus und der Vernetzung akademischer Datenbanken mit Zugang zu allen molekulardiagnostischen Ergebnissen der Patienten unter Berücksichtigung der nationalen und internationalen Vorgaben des Datenschutzes”, so Wörmann.
Das vollständige Positionspapier der medizinischen Fachgesellschaften kann unter folgender Internetadresse heruntergeladen werden: https://dgho.de/publikationen/stellungnahmen/gute-aerztliche-praxis/molekulare-diagnostik/molekulare-diagnostik-positionspapier-2019-1.pdf
Quelle: Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie e.V. (DGHO)
Brustkrebs: Höhere Dosis im Tumorgebiet bringt auch nach zwanzig Jahren bessere Tumorkontrolle für viele Patientinnen
Die Strahlentherapie nach einer brusterhaltenden Operation ist eine hocheffektive Behandlungsmethode. Eine Dosissteigerung – „Boost“ genannt – im ehemaligen Tumorbereich kann verhindern, dass es an der operierten Brust erneut zum Krebswachstum kommt. Dies bestätigt nun eine europäische Langzeitstudie, in der die Ergebnisse der Studienteilnehmerinnen 20 Jahren nach der Erkrankung ausgewertet wurden. Nach Einschätzung der Deutschen Gesellschaft für Radioonkologie (DEGRO) zeigt die Studie deutlich, dass viele Patientinnen von dieser höheren Dosis profitieren, insbesondere Frauen unter 50 und Frauen mit speziellen zusätzlichen histologischen Veränderungen, einem sogenannten DCIS.
Ein Brustkrebs im Frühstadium kann heute brusterhaltend operiert werden. „Zum Behandlungsstandard gehört heutzutage eine Bestrahlung, da es sonst zu einem Lokalrezidiv, also einem erneuten Burstkrebswachstum an der operierten Brust, kommen kann“, erläutert Professor Stephanie E. Combs von der Technischen Universität München.
Prof. Dr. Stephanie E. Combs, Direktorin der Klinik und Poliklinik für RadioOnkologie und Strahlentherapie am Universitätsklinikum der Technischen Universität München (TUM). Foto: DEGRO Deutsche Gesellschaft für Radioonkologie e.V.Um die optimale Dosis zu bestimmen, hat die European Organization for Research and Treatment of Cancer (EORTC) zwischen 1989 und 1996 eine Studie an 5.569 an Brustkrebs erkrankten Frauen durchgeführt. „Die Hälfte der Patientinnen erhielt damals neben der üblichen eine zusätzliche Bestrahlung der operierten Brust im Bereich des Tumorbettes die wir als Boost bezeichnen“, sagt die Pressesprecherin der DEGRO. Der Boost verlängere die Behandlungszeit zwar um knapp zwei Wochen, er könne aber ein Lokalrezidiv verhindern.
Die Teilnehmerinnen der EORTC-Studie werden seit dem Ende der Behandlung regelmäßig nachuntersucht, um herauszufinden, für welche Patientinnen der Boost den größten Nutzen bringt. Schon in den ersten Jahren zeigte sich, dass Frauen mit ungünstigen Gewebemerkmalen, sogenannten „high-grade“-Tumoren, den größten Nutzen haben. Dies konnte auch noch nach 20 Jahren bestätigt werden. Die Langzeitanalyse zeigt nochmals deutlich, dass prinzipiell alle Frauen von einer Dosisaufsättigung profitieren können. Der größte Vorteil zeigt sich für jüngere Patientinnen unter 50 Jahre. Sie erlitten nach einer Boost-Bestrahlung signifikant seltener ein Lokalrezidiv an der operierten Brust. Insgesamt jedoch profitieren alle Altersgruppen von einer Boostbestrahlung. Die zweite Gruppe sind Patientinnen, bei denen der Pathologe in der Nähe des invasiven Karzinoms die Krebsvorstufe DCIS gefunden hat. Bei duktalen Carcinoma in situ (DCIS) liegen in den Milchgängen der Brustdrüse veränderte Zellen vor, die aber noch am Ort verbleiben. „Die DCIS können noch keine Metastasen bilden“, sagt DEGRO-Präsident Professor Dr. med. Dr. rer. nat. Jürgen Debus. „Wenn DCIS-Nester in der Nähe des Primärtumors gefunden werden, ist es jedoch möglich, dass es später zu einem Lokalrezidiv kommt“, fügt Debus hinzu.
 Prof. Dr. Jürgen Debus
DEGRO Präsident und
Ärztliche Direktor der Klinik für RadioOnkologie
und Strahlentherapie (Czerny-Klinik)
am Universitätsklinikum Heidelberg
Foto: DEGRO Deutsche Gesellschaft für Radioonkologie e.V.
Prof. Dr. Jürgen Debus
DEGRO Präsident und
Ärztliche Direktor der Klinik für RadioOnkologie
und Strahlentherapie (Czerny-Klinik)
am Universitätsklinikum Heidelberg
Foto: DEGRO Deutsche Gesellschaft für Radioonkologie e.V.
Die EORTC-Studie liefert den Beweis, dass der Boost für die beiden Patientinnengruppen von erheblichem Vorteil ist: Bei jüngeren Frauen mit DCIS in der Nähe des Primärtumors verringerte die Boost-Bestrahlung die Rate von Lokalrezidiven an der operierten Brust von 31 auf 15 Prozent, halbiert sie also. Die Verlaufskurven lassen sogar vermuten, dass die Vorteile sich nach Ablauf von 20 Jahren noch weiter verstärken könnten. „Die EORTC-Studie zeigt, wie notwendig eine lange Nachsorge ist. Diese Langzeitdaten sind gerade für die jungen Patientinnen sehr wichtig. Prinzipiell ist ein Boost jedoch bei allen Frauen sinnvoll“, sagt Debus.
Literatur:
Vrieling C et al. Prognostic Factors for Local Control in Breast Cancer After Long-term Follow-up in the EORTC Boost vs No Boost Trial: A Randomized Clinical Trial. JAMA Oncology 2017; 3: 42-48. Abstract
Quelle: DEGRO Deutsche Gesellschaft für Radioonkologie e.V. – Internet: www.degro.org
Was den Patienten gut tut – Integrative Onkologie
„Die integrative Onkologie steht auf dem Boden der wissenschaftlichen, fundierten Medizin und stellt den Patienten mit seiner Perspektive und seinen Lebenszielen in den Vordergrund‘‘, betont Prof. Dr. Jutta Hübner. Das Ziel ihres Faches sieht Professorin Hübner in der auf die Bedürfnisse des Patienten abgestimmten Therapie als eine Kombination aus schulmedizinischen und sinnvollen ergänzenden Behandlungsmöglichkeiten.
 Prof. Dr. Jutta Hübner, Stiftungsprofessur für integrative Onkologie, Universitätsklinikum Jena
Prof. Dr. Jutta Hübner, Stiftungsprofessur für integrative Onkologie, Universitätsklinikum Jena
Über die Hälfte der Krebspatienten versucht neben der vom Arzt verordneten Strahlen- oder Chemotherapie auch pflanzliche Stoffe, Nahrungsergänzung oder Naturheilmittel, die in bunten Zeitschriften angepriesen oder in online-Erfahrungsberichten positiv bewertet werden. Bei den Brustkrebspatientinnen liegt dieser Anteil noch weit höher. „Für die Wirksamkeit der ergänzenden Mittel oder Methoden gibt es nur minimale Nachweise, und oft erfährt der behandelnde Arzt nichts von dieser Selbstbehandlung“, nennt Jutta Hübner gleich zwei zentrale Probleme dabei. Die Internistin hat seit diesem Jahr die Professur für Integrative Onkologie am Universitätsklinikum Jena inne, die die
Deutsche Krebshilfe als Stiftungsprofessur an der Klinik für Innere Medizin II eingerichtet hat und die direkt an das Universitätstumorzentrum angebunden ist.
Vor allem in der Onkologie, aber auch bei anderen chronischen vielschichtigen Krankheitsbildern ist der Bedarf an ergänzenden oder alternativen Behandlungsmöglichkeiten sehr groß – vor allem, wenn man körperliche Aktivität, Psychoonkologie oder Selbsthilfegruppenarbeit mit dazu zählt. „Und die komplementäre Medizin hat durchaus das Potential, den Patienten zu helfen‘‘, so Jutta Hübner. Als Beispiele zählt sie Ingwer gegen die Übelkeit bei Chemotherapie auf oder Yoga und leichten Sport zur Abmilderung des Erschöpfungszustandes Fatigue. Neben qualitativ hochwertigen Studien fehlt es vor allem an fundierten Informationen über komplementäre Behandlungsmöglichkeiten, sowohl bei den
Patienten, als auch bei den Ärzten.
Hier will Professorin Jutta Hübner, die zuvor eine Informationsdatenbank der Deutschen Krebsgesellschaft und der Deutschen Krebshilfe aufgebaut hat, mit einem niederschwelligen Angebot ansetzen. In regelmäßigen Vorträgen für Krebspatienten, Angehörige und Interessenten wird sie am Uniklinikum Jena über die Möglichkeiten und Risiken komplementärer Medizin informieren. In der Patientenversorgung führt sie die Arbeit der Ambulanz für Naturheilkunde und Integrative Onkologie an der Klinik für Innere Medizin II des Uniklinikums fort und plant, einen Konsildienst für stationäre Patienten des Klinikums zu etablieren.
Neben der Versorgungsforschung zum Informationsbedarf von Patienten zur komplementären und alternativen Medizin und zur Arzt-Patienten-Kommunikation, die gerade in der Onkologie auch zentrale medizinethische und medizinökomische Aspekte berührt, liegt der wissenschaftliche Schwerpunkt von Jutta Hübner in der evidenzbasierten Untersuchung komplementärer Medizin. „Gute Studienkonzepte in der Komplementärmedizin sind sehr aufwendig, dazu sind Netzwerke notwendig und eine Forschungskultur, zu deren Etablierung ich beitragen möchte‘‘, so Jutta Hübner.
Nach dem Medizinstudium in Düsseldorf absolvierte Jutta Hübner die Facharztausbildung in Innerer Medizin in Remscheid. Sie spezialisierte sich für die Hämatologie und internistische Onkologie und erwarb Zusatzqualifikationen in der Chirotherapie, Palliativmedizin, Naturheilkunde und Psychoonkologie. Nach klinischen Leitungspositionen in Bad Soden-Salmünster, Kassel und am Universitätsklinikum Frankfurt/Main arbeitete sie bei der Deutschen Krebsgesellschaft und habilitierte sich an der Friedrich-Schiller-Universität Jena zum Stand und der Zukunftsperspektive der integrativen Onkologie.
Quelle: Universitätsklinikum Jena
Stammzellforschung – Von der Krebsursache zum medizinischen Fortschritt
Zum nunmehr sechsten mal richtet das Deutsche Krebsforschungszentrum (DKFZ) vom 18. bis 20. September 2016 das Internationale Heinrich F.C. Behr-Symposium aus, dass alle zwei Jahre stattfindet. Rund 400 Experten aus aller Welt tauschen sich aus, um über Stammzellen, Krebs und Krebsstammzellen zu berichten und zu diskutieren.
“…Wir sind davon überzeugt, dass dieses Forschungsgebiet die Behandlung von Krebspatienten in Zukunft entscheidend beeinflussen und verbessern wird”, sagt Michael Boutros, der kommissarische Wissenschaftliche Vorstand des DKFZ. “Das zeigen allein schon einige der Ergebnisse, die auf dem diesjährigen Symposium vorgestellt werden.” “Die Krebsstammzellforschung ist in der Medizin angekommen”, freut sich Andreas Trumpp vom DKFZ und von HI-STEM, dem “Heidelberger Institut für Stammzellforschung und experimentelle Medizin, das das DKFZ mit der Dietmar Hopp Stiftung gegründet hat. “Die Aufklärung der Tricks der Krebsstammzellen liefert uns wertvolle Ideen für die Therapie, die wir nun beginnen umzusetzen. Und mit 3D-Kulturen von Tumoren können wir das Tumorgeschehen in der Petrischale nachahmen und gleichzeitig Strategien für die Behandlung entwickeln.”
Erblich bedingten Brustkrebs
Von der Stammzellforschung zur Brustkrebs-Prävention – das ist das Ziel von Jane Visvader vom Walter and Eliza Hall Institute in Melbourne, Australien. 2006 ist es ihr als erster gelungen, die Brustdrüsen-Stammzellen zu identifizieren. Nun hat sie herausgefunden, wie genetische Veränderungen bestimmte Tochterzellen dieser Stammzellen zu einer besonders gefährlichen Form von Brustkrebs entarten lassen, und wie man diesen Prozess mit einem Medikament verhindern kann. Dies könnte die Prävention von erblich bedingtem Brustkrebs erheblich verbessern, als Alternative zur bisher oft vorgenommenen Radikaloperation.
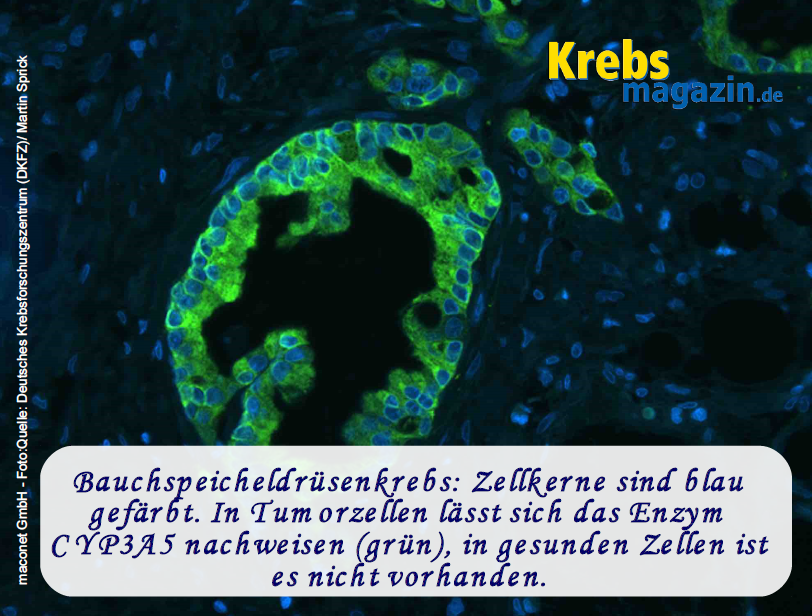
Bauchspeicheldrüsenkrebs
Andreas Trumpp berichtet darüber, wie verschiedene Krebsstammzellen unterschiedliche Typen von Bauchspeicheldrüsenkrebs hervorrufen. Auf der Basis dieser Forschung fand er heraus, warum einer der Subtypen von Bauchspeicheldrüsenkrebs so besonders resistent gegen Chemotherapien ist und wie sich hieraus ein neuer Ansatz ergeben könnte, um wirksamere Therapien zu entwickeln.
Organoide zum besseren Verständnis für Organentwicklung und Krankheitsentstehung
Ein besonders spannendes Thema der aktuellen Stammzellforschung sind so genannte Organoide, in der Kulturschale aus Stammzellen gezüchtete organähnliche Strukturen. Für die Grundlagenforschung haben sie großes Potential, um beispielsweise zu verstehen, wie sich Organe entwickeln oder wie Krankheiten entstehen. In der medizinischen Forschung verspricht man sich Fortschritte bei der Entwicklung von Organersatz, sie gelten außerdem als ideal, um neue Wirkstoffe zu erproben.
Gehirn in der Kulturschale
Jürgen Knoblich vom Institut für Molekulare Biotechnologie in Wien stellt das besonders aufsehenerregende und hochkomplexe menschliche “Gehirn in der Kulturschale” vor, das tatsächlich aus verschiedenen gehirntypischen Strukturen aufgebaut ist und aktive Nervenzellen enthält.
Organoide aus patienteneigenen Krebszellen zur zielgerichteten Therapie
Dem niederländischen Stammzellforscher Hans Clevers vom Hubrecht Institut für Entwicklungsbiologie und Stammzellforschung in Utrecht ist es erstmals gelungen, Organoide aus patienteneigenen Krebszellen zu züchten. An diesen Gewebestrukturen können die Wissenschaftler und Ärzte prüfen, welche zielgerichteten Medikamente oder Medikamentenkombinationen am wirksamsten sind und so die Therapie vorab an den individuellen Tumor anpassen.
Quelle: Deutsches Krebsforschungszentrum (DKFZ), Internationale Heinrich F.C. Behr-Symposium, 18. bis 20. September 2016
Brustkrebs Metastasierung – Protein Endosialin als möglichen Biomarker identifiziert
Wissenschaftler aus dem Deutschen Krebsforschungszentrum haben gemeinsam mit Londoner Kollegen entdeckt, dass das Protein Endosialin eine Schlüsselrolle bei der Metastasierung von Brustkrebs spielt. Produzieren bestimmte Zellen der Blutgefäßwand viel Endosialin, so können Brustkrebszellen leichter in die Blutbahn eindringen und sich so im Körper ausbreiten. Die Forscher sehen in Endosialin einen potentiellen Biomarker, um das Risiko für die Metastasierung einzuschätzen. Wirkstoffe gegen Endosialin könnten möglicherweise sogar die Metastasierung aufhalten.
Wenn Brustkrebs in andere Gewebe des Körpers streut, sinken die Chancen auf Heilung rapide. Metastasen, die Tumorabsiedlungen, sind die Hauptursache für die knapp 18.000 jährlichen Brustkrebs-Todesfälle in Deutschland – der primäre Krebsherd ist selten tödlich.
Weil sie auf die Versorgung mit Nährstoffen angewiesen sind, locken Tumoren Blutgefäße aktiv an. Außerdem nutzen Krebszellen die Blutgefäße, um sich im Körper zu verbreiten. Eine Gruppe von Forschern um Hellmut Augustin vom Deutschen Krebsforschungszentrum und der Medizinischen Fakultät Mannheim der Universität Heidelberg hat nun gemeinsam mit Kollegen um Clare Isacke vom Institute of Cancer Research in London untersucht, wie die Blutgefäße die Krebsausbreitung aktiv unterstützten. Eine zentrale Rolle spielen dabei die so genannten Perizyten, Zellen, die das Äußere der Gefäße bedecken.
Den Forschern war aufgefallen, dass Perizyten große Mengen des Membranproteins Endosialin produzieren. Um eine mögliche Rolle dieses Moleküls bei der Ausbreitung von Krebszellen zu prüfen, verglichen sie Mäuse, die aufgrund eines Gendefekts kein Endosialin produzieren konnten, mit normalen Tieren.
Während Endosialin für das Wachstum der primären Brusttumoren keine Rolle spielte, fördert es stark deren Metastasierung. Offenbar erleichtert es Endosialin den Tumorzellen, mit den Gefäßzellen in Kontakt zu treten und so in die Blutbahnen einzudringen. Das konnten die Wissenschaftler an Experimenten mit Tumorzellen und Blutgefäßzellen in der Kulturschale direkt mitverfolgen.
Um herauszufinden, ob sich auch bei Brustkrebspatientinnen ein Zusammenhang zwischen Endosialin und der Ausbreitung der Erkrankung beobachten lässt, untersuchte das Forscherteam Tumor-Gewebeproben von 334 Patientinnen. Beim Abgleich mit den klinischen Verläufen stellten die Wissenschaftler fest: Je höher die Endosialin-Spiegel in den Tumor-Blutgefäßen war, desto stärker hatte der Krebs gestreut. Auch die Überlebenszeit stand im Zusammenhang mit der Menge des von den Perizyten produzierten Endosialins.
“Wir wissen noch nicht, warum und wann Perizyten plötzlich damit beginnen, große Mengen Endosialin zu produzieren. Und wir wissen auch noch nicht, wie das Molekül den Krebszellen tatsächlich dabei hilft, die Blutgefäße zu entern. Das werden die kommenden Schritte unserer Forschung sein”, sagt Courtney König, die Erstautorin der Arbeit.
Studienleiter Hellmut Augustin ergänzt: “Es lohnt sich zu prüfen, ob sich Endosialin als Biomarker eignet, der das Risiko der Metastasierung anzeigt: Wird in der Tumorgewebeprobe einer Brustkrebspatientin viel Endosialin gefunden, so könnte das bedeuten, dass der Tumor bereits gestreut hat. Darüber hinaus werden zukünftige Arbeiten zeigen, ob ein Wirkstoff gegen Endosialin die Metastasierung bremsen kann.”
Literaturhinweise:
Carmen Viski, Courtney König, Magdalena Kijewska, Carolin Mogler, Clare M. Isacke, and Hellmut G. Augustin: Endosialin-expressing Pericytes Promote Metastatic Dissemination.
Cancer research 2016, DOI: 10.1158/0008-5472.CAN-16-0932
Quelle: Deutsches Krebsforschungszentrum (DKFZ)
DKK 2016: Der informierte Patient – Individuell beraten, gemeinsam entscheiden

Broschüre als download beim Bundesgesundheitsministerium: “Nationaler Krebsplan” :
Um Betroffene in Deutschland bestmöglich zu unterstützen, hat die Deutsche Krebshilfe ihren telefonischen Beratungsdienst modernisiert. Seit Oktober 2014 können Ratsuchende die Mitarbeiter und Mitarbeiterinnen des INFONETZ KREBS kontaktieren. Die kostenfreie Beratung beruht dabei auf einer Datenbank nach aktuellem Stand der Medizin und Wissenschaft, die in Zusammenarbeit mit der Deutschen Krebsgesellschaft entwickelt wurde. „Im vergangenen Jahr haben die Beraterinnen und Berater des INFONETZ KREBS insgesamt rund 10.000 Gespräche geführt und schriftliche Anfragen beantwortet. Eine Zahl, die uns den großen Informationsbedarf nochmal eindrucksvoll bestätigt und uns außerdem zeigt, welch großes Vertrauen Betroffene in Deutschland dem INFONETZ KREBS entgegenbringen“, so Nettekoven.
Für viele Betroffene ist das Internet häufig das erste Recherchemittel. Es hält jedoch eine wahre Flut an Informationen bereit, und nur schwer lässt sich zwischen seriösen und interessengesteuerten Aussagen unterscheiden. „Schon auf der ersten Seite der Suchmaschine tauchen außerdem alle Reiz- und Schreckenswörter auf“, beschreibt Andrea Hahne, Vorstandsvorsitzende vom BRCA-Netzwerk – Hilfe bei Familiärem Brust- und Eierstockkrebs, die Situation aus der Sicht einer Betroffenen. Als kompetente Ansprechpartner nennt sie in diesem Zusammenhang auch die Krebsselbsthilfe-Organisationen, die bei der Beratung auf eigene Erfahrungen zurückgreifen und damit authentisch berichten können.
Für die behandelnden Ärzte auf der anderen Seite besteht eine besondere Herausforderung darin, statistische Zusammenhänge zu erfassen und ihren Patienten zu vermitteln. Aussagen wie „Die relative Überlebensrate liegt bei 57 %“ oder „Die Rezidivwahrscheinlichkeit beträgt 12 %“ können Patienten nur schwer einordnen. Selbst für Ärzte sind statistische Angaben mitunter schwer abzuwägen. „Mangelndes Verständnis für Statistik kann aber leicht zu falschen Entscheidungen führen“, erklärte Professor Dr. Gerd Gigerenzer, Direktor des Harding Zentrums für Risikokompetenz und des Forschungsbereichs Adaptives Verhalten und Kognition am Berliner Max-Planck-Institut für Bildungsforschung. Eine fundierte statistische Ausbildung von Medizinstudenten und bereits praktizierenden Ärzten sei daher dringend erforderlich.
Zu wenig Zeit für den einzelnen Patienten auf Seiten der Ärzte und der Pflege, häufig wechselnde Behandler und mangelnde Teamkommunikation behindern aktuell den Prozess des gemeinsamen Entscheidens. Dies stellte Dr. Isabelle Scholl vom Institut und Poliklinik für Medizinische Psychologie des Universitätsklinikums Hamburg-Eppendorf in einer Studie fest. „Nur selten werden Therapieentscheidungen heute gemeinsam von Arzt und Patient getroffen“, erklärte Scholl. Um dieses Problem anzugehen, hat sie ein Programm entwickelt, das helfen soll, die gemeinsame Entscheidungsfindung in den medizinischen Alltag zu integrieren.
Krebs ist eine Erkrankung, die überwiegend im höheren Alter auftritt. Ältere Patienten haben oft eine Vielzahl von Gesundheitsproblemen und Funktionseinschränkungen, die eine entsprechende Unterstützung notwendig machen. „Die ohnehin schwierige Aufklärung eines Patienten über Diagnose und Therapieoptionen bei einer Krebserkrankung wird oft zusätzlich durch kognitive Einschränkungen des Patienten und die Notwendigkeit der Aufklärung von Angehörigen erschwert“, erklärte Prof. Dr. Elisabeth Steinhagen-Thiessen, Geriaterin an der Charité – Universitätsmedizin Berlin. „Wir brauchen eine vertrauensvolle fächerübergreifende Zusammenarbeit der Onkologie, Palliativmedizin und Geriatrie, um die Herausforderungen bei älteren onkologischen Patienten zu meistern und optimal behandeln zu können.“
Quelle: Deutscher Krebskongress 2016 – Veranstalter: Stiftung Deutsche Krebshilfe / Deutsche Krebsgesellschaft e.V.
DKK 2016: Krebsprävention: Vernachlässigter Bereich unseres Gesundheitswesens?
Krebsprävention und Krebsfrüherkennung sind die wichtigste Basis für ein Leben ohne Krebs. Angesichts steigender Neuerkrankungszahlen müsse in Deutschland jedoch deutlich mehr als bislang in diesen Bereichen getan werden, so das Experten-Fazit auf einer Pressekonferenz anlässlich des Deutschen Krebskongresses 2016. Auf der Veranstaltung wurden aktuelle Erkenntnisse aus der Präventionsforschung vorgestellt und Maßnahmen aus dem Bereich der Primärprävention, der Früherkennung und der Prähabilitation diskutiert.
„Wir haben mittlerweile Belege dafür, dass eine nachhaltige Änderung des Lebensstils tatsächlich etwas bringt. Wer zum Beispiel mit dem Rauchen aufhört oder bei einem Body-Mass-Index von mehr als 30 sein Gewicht reduziert, der kann auch tatsächlich sein Krebsrisiko senken“, erklärte Prof. Dr. Olaf Ortmann, Mitglied des Vorstands der Deutschen Krebsgesellschaft auf der Veranstaltung. Jetzt gehe es vor allem darum, die entsprechenden Umsetzungsmaßnahmen zu formulieren, sowohl für die Aufklärung der Bevölkerung als auch zur Risikovermeidung. „Leider wissen wir zu wenig darüber, wie wir große Bevölkerungsgruppen nachhaltig zur Vermeidung von Risiken motivieren und dabei unterstützen können. Hier ist deutlich mehr wissenschaftliche Forschung notwendig“, so Ortmann.
Für strukturierte und qualitätskontrollierte Konzepte zur risikoadaptierten Prävention bei erblich bedingten Krebserkrankungen plädierte Prof. Dr. Rita Schmutzler, Direktorin des Zentrums Familiärer Brust- und Eierstockkrebs in Köln. Schätzungsweise bei einem Drittel aller Brust-, Darm- und Prostatakrebserkrankungen sind genetische Risikofaktoren im Spiel. Bis vor kurzem waren nur einige Hochrisikogene wie BRCA1 und BRCA2 bekannt, die jedoch nur einen Teil dieser erblich bedingten Fälle erklären. Mit den neuen technischen Möglichkeiten der genomweiten Analyse werden gegenwärtig eine Reihe weiterer Risikogene identifiziert, die in Zukunft eine präzisere und individuelle Risikoberechnung ermöglichen werden. Dies betrifft nicht nur das Erkrankungsrisiko, sondern auch Informationen über den spezifischen Tumorsubtyp. Prinzipiell kann dadurch die Effektivität von Früherkennungsprogrammen, wie z. B. das Mammographiescreening deutlich verbessert werden. Doch bei welchem Risiko oder Tumorsubtyp sind welche klinischen Maßnahmen nötig? Für welche Patientin kommt wann welche Früherkennung infrage? Schmutzler: „Angesichts dieser komplexen Fragen brauchen wir eine qualitätsgesicherte Gendiagnostik, die den Bogen vom Labor bis in die Klinik spannt und sich auf aussagekräftige Studien stützt. Die Grundvoraussetzung dafür sind neu zu errichtende Register zu familiären Tumorerkrankungen, um die Effektivität unserer Präventionsmaßnahmen bei erblichen Krebserkrankungen zu erfassen und kontinuierlich zu messen.“
Wie wichtig es ist, Früherkennungsmaßnahmen durch Forschung zu begleiten, zeigen die Studien von Prof. Dr. Hermann Brenner vom Deutschen Krebsforschungszentrum in Heidelberg. Brenner, der Preisträger des Darmkrebs-Präventionspreises 2015, untersucht die Wirksamkeit der Darmkrebsfrüherkennung seit mehr als zehn Jahren. Durch seine Untersuchungen konnte er z. B. zeigen, dass bis zu 90 Prozent der Darmkrebsfälle durch eine Vorsorge-Koloskopie verhütet werden könnten und das Darmkrebsrisiko nach einer Vorsorgekoloskopie ohne auffälligen Befund über mehr als zehn Jahre sehr niedrig ist. Dieses Ergebnis unterstützt die derzeitige Praxis eines Zehn-Jahres-Intervalls bei der Vorsorge-Koloskopie. Trotz dieser Bestätigung ist die Akzeptanz für die Vorsorge-Koloskopie in der Bevölkerung nach wie vor niedrig. Deshalb gehe es vor allem darum, organisierte Einladungsverfahren zu implementieren, in denen die berechtigten Versicherungsnehmer individuell angesprochen und über die verfügbaren Screeningverfahren aufgeklärt werden. „Außerdem müssen neue Methoden evaluiert werden, die die Akzeptanz des Screenings in der Bevölkerung erhöhen“, so Brenner.
Anders als beim Darmkrebs gibt es beim Lungenkrebs bislang noch kein geeignetes Screeningverfahren. Einer amerikanischen Studie zufolge kann zwar eine jährliche Mehrschicht-Computertomographie (MSCT) die Lungenkrebs-Sterblichkeit bei starken Rauchern um 20 Prozent senken. Doch die Rate falsch positiver Ergebnisse ist hoch, d. h. manche Teilnehmer müssen wieder einbestellt werden, um verdächtige Befunde zu überprüfen, die sich dann gar nicht als Lungenkrebs herausstellen. Die Ergebnisse der LUSI-Studie, einer randomisierten kontrollierten Studie mit mehr als 4.000 Teilnehmern, zeigen, dass der falsche Alarm ab der zweiten Screening-Runde unter bestimmten Bedingungen abnehmen kann. „Verdächtige Befunde im ersten CT, die sich in der darauffolgenden Untersuchung nicht verändert haben, sind offensichtlich keine Krebsherde. Eine erneute Abklärung ist deshalb nicht mehr notwendig“, erklärt LUSI-Studienleiter Prof. Dr. Nikolaus Becker vom DKFZ Heidelberg. Allerdings gehen die „falschen Alarme“ nur zurück, wenn die Vorbefunde früherer Screeningrunden für diese Beurteilung vorliegen, ein Lungenkrebs-Screening also als „organisiertes Screening“ durchgeführt würde. Die Endauswertung von LUSI und anderen europäischen Studien zur Lungenkrebsfrüherkennung ist für die nächsten ein bis zwei Jahre geplant.
Vorbeugen hilft möglicherweise auch dann noch, wenn der Krebs schon diagnostiziert ist, so PD Dr. Freerk Baumann von der Sporthochschule Köln. Dieses junge Forschungsfeld wird unter dem Begriff Prähabilitation zusammengefasst und steht für das Verbinden von Prävention und Rehabilitation. Das Konzept: Eine rechtzeitige bewegungstherapeutische Intervention unmittelbar nach der Krebsdiagnose soll die Patienten körperlich auf die Therapiephase vorbereiten. Nach dem Motto „Fit für die Krebsbehandlung“ wollen die Wissenschaftler so möglichen Komplikationen und Nebenwirkungen vorbeugen. „Erste Daten zeigen, dass die Prähabilitation nicht nur die Nebenwirkungen der Krebsmedikamente verhindert, sondern auch die Therapiedosierung während der Behandlung beibehalten werden kann. Außerdem lassen sich Krankenhaustage reduzieren“, betonte Baumann.
Quelle: Deutscher Krebskongress DKK 2016
TOP-Infos zu modernen Krebsmedikamenten: Arzneimittel bewertung wird neue Rubrik auf Onkopedia.com
 Prof. Dr. Diana Lüftner, Oberärztin an der Medizinischen Klinik mit Schwerpunkt Hämatologie und Onkologie an der Berliner Charité.
Prof. Dr. Diana Lüftner, Oberärztin an der Medizinischen Klinik mit Schwerpunkt Hämatologie und Onkologie an der Berliner Charité.