| Targeted Therapy Den Tumor im Visier  Prof. Hans-Jochen Illiger, Herausgeber Krebsmagazin, Klinikum Oldenburg gGmbH Prof. Hans-Jochen Illiger, Herausgeber Krebsmagazin, Klinikum Oldenburg gGmbHDas Spektrum target orientierter Therapien hat sich in den letzten Jahren erheblich erweitert und so sind denn auf dem diesjährigen ASCO-Meeting viele Arbeiten präsentiert worden, die sich mit der klinischen Wirkung dieser Substanzen beschäftigten. Und aus zunächst nur hoffnungsvoll erscheinenden Ansätzen haben einige Substanzen den Eingang in die Routine gefunden und sind unter bestimmten Voraussetzungen inzwischen auch in Europa zugelassen. Der Wirkstoff Bortezomib in der Therapie des Multiplen Myeloms (Plasmozytom). Für den Abbau von Proteinen die das Zellwachstum regulieren, spielen Proteasome in Zellen eine wichtige Rolle. Hier setzt der Wirkstoff Bortezomib als Protease – Hemmer an, der die Stoffwechselwege der bösartigen Krebszellen, die ein eigenständiges Wachstum haben blockiert. Auf dem zurückliegenden ASCO stellte P.G. Richardson vom Dana Farber Institut in Boston Zwischenergebnisse einer wissenschaftlichen Studie vor, bei der 657 vorbehandelte Patienten mit Multiplen Myelom einbezogen waren und bei der eine Gruppe von 327 Patienten Bortezomib erhielt, die mit einer anderen Gruppe verglichen wurde, die mit Dexamethason behandelt wurde.  RR = Ansprechrate; Toxizität = Giftigkeit. Insgesamt 15 der mit Bortezomib behandelten Patienten erreichten eine komplette Remission gegenüber nur 5 Patienten in der Dexamethason-Gruppe. Die Zeit bis zum Fortschreiten der Erkrankung stieg um 58% und auch beim Gesamtüberleben zeigten sich deutliche positive Trends zu Gunsten von Bortezomib mit insgesamt 13 im Vergleich zu 24 Todesfällen in der Dexamethason-Gruppe. Das Nebenwirkungsprofil zeigte bei Bortezomib mehr gastrointestinale, neurologisch, allgemeine, kardiale und hämatologische Nebenwirkungen als Dexamethason. Inzwischen ist Bortezomib in Europa für Patienten mit Multiplen Myelom zugelassen, die zuvor mindestens zweimal behandelt wurden und bei denen die Krankheit während der letzten Therapie einen Fortschritt zeigte. Wirkstoff Rituximab in der Therapie seltener Non-Hodgkin-Lymphome Bei Rituximab handelt es sich um einen monoklonalen Antikörper der gegen CD20 gerichtet ist. Antikörper sind Abwehrstoffe und werden z.B. gebildet, wenn ein fremder Stoff wie Bakterien in den Körper gelangt. Antikörper sind von weißen Blutkörperchen erzeugte Proteine. 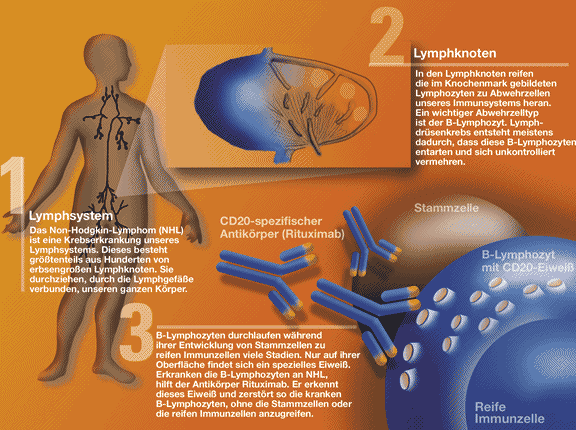 Prof. Dr. M.G. Pfreundschuh stellte beim diesjährigen ASCO die Studie einer internationalen Arbeitsgruppe vor, bei der 770 Patienten im Alter von 18-60 Jahren mit einem niedrig malignen diffusen Large B-Zell-Lymphom - einer seltenen Form des Non-Hodgkin-Lymphom behandelt wurden. Nach 15 Monaten waren in der Rituximab Gruppe 84% im Vergleich zu 62,5% der Patienten die nach dem herkömmlichen CHOP-Schema behandelt wurden ohne ein Fortschreiten ihrer Erkrankung. Auch die Quote der kompletten Remissionen war mit 84,7% im Vergleich zu 66% sowie die Rate bis zum erneuten Fortschreiten der Erkrankung mit 6,3% gegenüber 17,7% günstiger und das Gesamtüberleben mit 98,5% gegenüber 92% überlegener. In einer weiteren Studie berichtete Prof. Dr. W. Hiddemann für eine Deutsche Arbeitsgruppe, dass beim Mantelzelllymphom durch die Zunahme von Rituximab in Ergänzung zum klassischen CHOP-Schema ebenfalls eine deutliche Prognoseverbesserung erreichbar ist. Leider ist das Mantelzelllymphom sehr schwierig zu behandeln. Patienten in der Regel im fortgeschrittenen Alter, haben eine schlechte Prognose mit einem mittleren Überleben von 3- 4 Jahren. 60 Patienten mit frisch diagnostiziertem Mantelzelllymphom im Stadium 3 und 4 erhielten eine Therapie nach dem CHOP Schemata, während 62 Patienten zusätzlich Rituximab erhielten. Die Quote kompletter Remissionen war mit 34 gegenüber 7%, die Gesamtansprechrate mit 94% gegenüber 75% und die Zeit bis zum Therapieversagen mit 22 gegenüber 14 Monaten zu Gunsten der Rituximab-Gruppe deutlich günstiger. Der Schluß, dass die kombinierte Chemo-Immun-Therapie den neuen Goldstandard zur Behandlung des Mantelzelllymphoms darstellt, liegt nahe, auch wenn die Anzahl von Knochenmarkschädigungen in der kombinierten Behandlungsgruppe etwas höher lag. Schließlich stellte H.S. Hochster die Daten einer weiteren Studie vor, bei der versucht wurde, bei indolenten Lymphomen nach erfolgter CVP Therapie (bestimmtes Behandlungsschema) mit Rituximab die Zeit bis zum Fortschreiten der Erkrankung zu verlängern. In der Studie wurden Patienten im Stadium 3 und 4 mit folikulären oder kleinzellig lymphozytischen Non HodgkinLymphom einbezogen die nach der Chemotherapie mit dem CVP Schema in zwei Gruppen aufgeteilt wurden. 154 Patienten erhielten Rituximab für 2 Jahre während 149 Patienten zunächst keine weitere Behandlung mehr erhielten. Das Überleben ohne Fortschreiten der Erkrankung betrug nach 2 Jahre 74% im Vergleich zu 42% zu Gunsten der Rituximab Gruppe. Auch nach 4 Jahren war es mit 58 gegenber 34% noch deutlich besser. Auch war die Verträglichkeit der Therapie insgesamt gut, so dass ein routinemäßiger Einsatz durchaus sinnvoll erscheint. Wirkstoff Gefitinib bei Tumoren der Lungen und Bronchien Gefitinib wird in der Fachsprache als EGFR Tyrosinkinase Inhibitor bezeichnet und stoppt Signale für Zellwachstum und -vermehrung. Dazu besetzt er besondere Rezeptoren in der Hülle der Krebszelle. Inzwischen konnten genetische Unterschiede identifiziert werden, die ein Ansprechen auf Gefitinib erwarten lassen, denn nur etwa 10% der Patienten mit Lungentumoren profitieren von dieser Substanz. H.J. West vom Schwedischen Cancer Institut in Seatle, USA, konnte darüber hinaus Daten einer Studiengruppe präsentieren, die bei fortgeschrittenem Lungenkrebs, bei denen Lungenbläschen und Bronchien betroffen waren, erhoben wurden. Von 35 vorbehandelten und 102 nicht vorbehandelten Patienten zeigten die Kurven für das Gesamtüberleben keinen Unterschied. Bemerkenswerter Weise ergaben sich geschlechtsspezifische Unterschiede: die durchschnittliche Überlebensrate für Frauen betrug 19 Monate und für Männer 8 Monate und auch die Ansprechrate war für Frauen mit 20% gegenüber 13% bei Männern günstiger. Für Patienten die einen Hautausschlag enwickelten, war das mittlere Überleben mit 13 gegenüber 5 Monaten und die Ansprechrate mit 21% gegenüber 0% ebenfalls deutlich günstiger. Und schließlich zeigte sich auch für Nichtraucher eine insgesamt bessere Prognose. Und so spekuliert man, das Gefitinib der neue Standard zur Behandlung bei Tumoren der Lungenbläschen und Bronchien (Bronchioloalveolarzellkarzinom) wird. Wirkstoff Cetuximab in der Therapie metastasierter kolorektaler Karzinome und Plattenepithelkarzinomen im HNO (Hals-Nasen und Ohren) Bereich Cetuximab ist ebenfalls ein monoklonaler Antikörper, der den Oberhaut (Epidermis) betreffenden Wachstumsfaktorrezeptor blockiert. Beim Plattenepithelkarzinom im HNO Bereich wurde diese Substanz in einer Studie in Kombination mit einer hochdosierten Strahlentherapie untersucht. Diese Kombination führte mit 54 Monaten im Vergleich zu 28 Monaten zu einer deutlichen Verlängerung der Überlebenszeit im Vergleich zur alleinigen Strahlenbehandlung. Beim metastasierten kolorektalen Karzinomen wurde Cetuximab in Ergänzung zu verschiedenen Chemotherapien untersucht. Unter anderem berichtet H.J. Lenz über die Aktivität von Cetuximab bei Patienten, die gegen Irinotecan und auch Oxaliplatin resistent geworden waren. Die Monotherapie mit Cetuximab führte bei 12% der Patienten zu einer Teilremission, während weitere 34% eine stabile Erkrankung für mindestens 6 Monate zeigten. Wirkstoff SU 11248 in der Therapie von Nierenzellkarzinomen und gastrointestinalen Stromatumoren SU 11248 ist ein Thyrosinkinase Inhibitor mit verschiedenen Angriffspunkten. Er richtet sich gegen den Tumor selbst, hat antiangiogenetische Aktivitäten und hemmt diverse Wachstumsfaktorrezeptoren. R.J. Motzer vom Memorial Sloan Catering Cancer-Center in New York untersuchte diese Substanz bei NierenzellkarzinomPatienten nach einer Standardvorbehandlung. Überraschend war das Ansprechen der Erkrankung auf diesen Wirkstoff. 21 von 63 Patienten erlebten eine teilweise Verbesserung ihrer Erkrankung, 23 eine mindestens 3 Monate dauernde Stabilisierung. Auch die durchschnittliche Zeit bis zum Fortschritt der Erkrankung wäre mit 8,3 Monaten mehr als doppelt so lang. Eine andere Indikation für SU 11248 könnten metastasierte gastrointestinale Stromatumoren sein, die dem Wirkstoff Imatinib gegenüber resistent sind, wie G.D. Demitri berichtete der vor allem den hohen klinischen Benefit von 54% für Patienten, die zuvor unter Imatinib ein Fortschreiten ihrer Erkrankung zeigten. Resumée Das Spektrum der Target - orientierten Therapien mit teilweise sehr positiven Ergebnissen läßt Hoffnung aufkommen, dass insbesondere die Erkrankungen, bei denen wir in der Vergangenheit so wenig erfolgreich waren, besser behandelt werden können. Doch viel Arbeit bleibt noch zu tun, insbesondere bei den Substanzen, die mehrere Targets zum Ziel haben, gilt es zu evaluieren, welche Wirkmechanismen letztlich entscheidend sind. |